これまでの疫学研究や病態生理に関する研究から、睡眠時無呼吸症候群は単なる循環器疾患の併存疾患というだけではなく、その発症や進展に直接的に関与するリスク因子であると考えられています。また、循環器疾患の発症後も睡眠時の無呼吸が存在すれば循環器疾患の増悪をきたし、より状態の悪い患者では中枢性無呼吸が更に悪化します。そのため、睡眠時無呼吸症候群は循環器疾患の一次・二次予防における介入のターゲットになっています。
睡眠時無呼吸症候群と循環器疾患
睡眠時無呼吸症候群が循環器疾患の発症と進展に寄与するメカニズム
睡眠時無呼吸症候群(Sleep Apnea Syndrome: SAS)は他の冠危険因子と同様に動脈硬化の進展に関わり、心血管イベントの発症に強く影響することが知られています。また、循環器疾患患者では上気道の閉塞に起因する睡眠時の無呼吸だけでなく、呼吸調節の異常に起因する中枢性の睡眠時無呼吸を呈する患者が多いことも知られています。中枢性睡眠時無呼吸症候群(Central Sleep Apnea Syndrome: CSA)は、特に心不全において頻度が高く、中枢性の無呼吸もしくは低呼吸と換気量が漸増漸減する過呼吸を周期的に繰り返すチェーンストークス呼吸を呈することが多く認められます。
各心血管疾患における睡眠時無呼吸症候群の合併頻度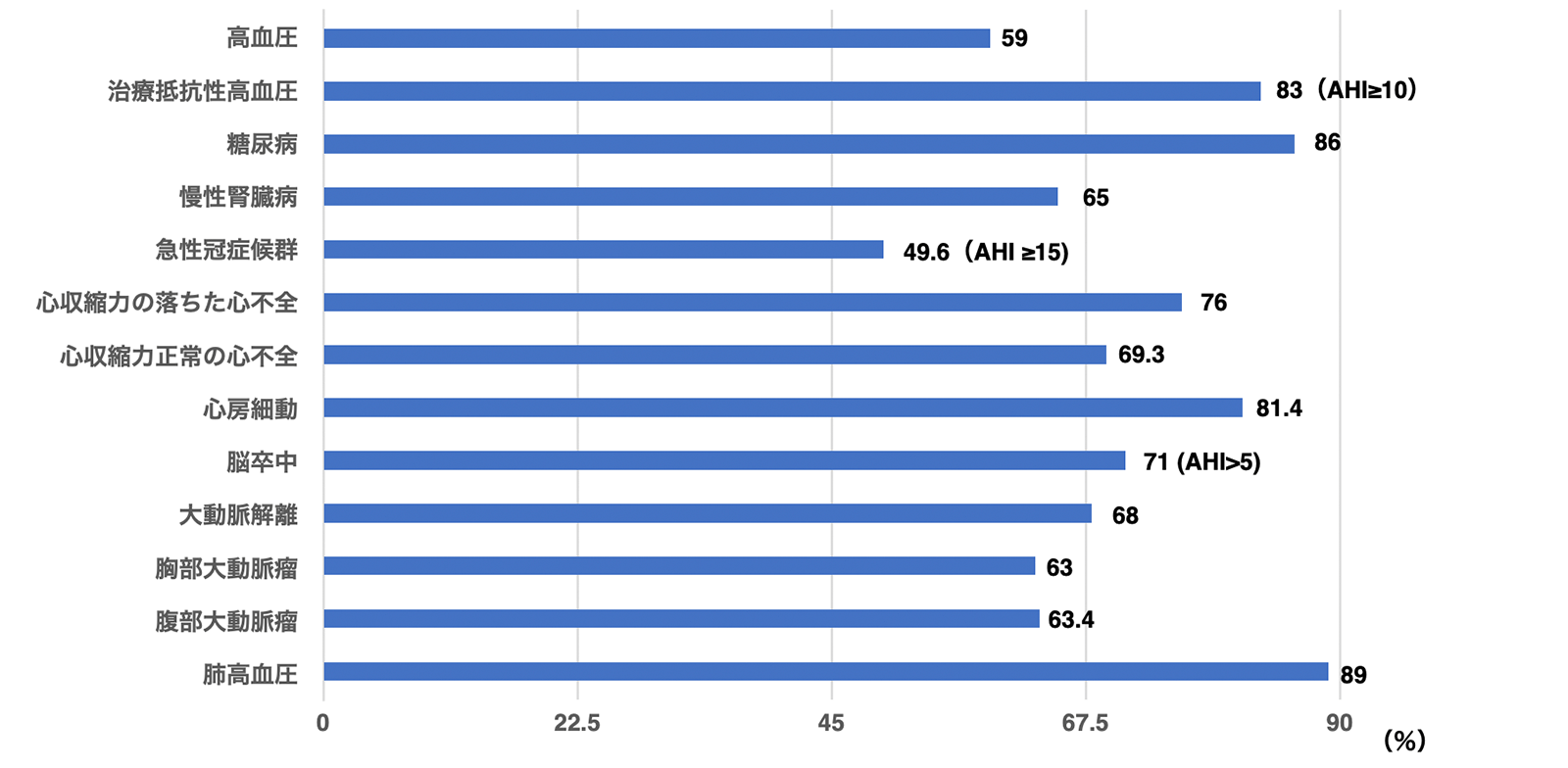
心血管疾患における閉塞性睡眠時無呼吸症候群(Obstractive Sleep Apnea Syndrome: OSA)の合併頻度は50%以上の高頻度であり、OSA合併例では心血管疾患に関する予後も不良であることが示されています。OSAでは上気道が閉塞している一方で呼吸努力はあるため胸腔内圧が陰圧となり、時に−50mmHg以上の陰圧が生じる状態を一晩中繰り返しますが、これは心臓の心室収縮に対して直接的に悪影響を与えています。一方、胸腔内が陰圧になると静脈還流が急速に増加して、右室容積が急激に増大することに加え、低酸素に伴う肺動脈の攣縮により圧負荷の増大もきたします。その結果として、重症例では心室中隔が左心室側に偏位して左心室の充満が妨げられ、心拍出量が一過性に低下します。
OSAと循環器疾患発症の病態生理
(Shamsuzzaman AS, et al. JAMA 2003より引用改変)
このような血行動態への変化には交感神経系の亢進も影響しており、交感神経活動の亢進は、高カテコールアミン状態による直接的神経障害、血圧上昇、心拍数増加、不整脈の誘発など心血管系全体へ影響します。また、無呼吸に伴い一過性に高度の低酸素状態と再酸素化を生じるため、OSA患者では酸化ストレスが亢進して血管内皮機能が障害されて動脈硬化が起こりやすくなりプラークの不安定化も起こします。このような状態が長期にわたると実際の動脈硬化として冠動脈疾患、心筋梗塞などが起こり、最終的には心不全に至ります。
心血管イベントの発症率
(Peker Y, et al. Am J Respir Crit Care 2002より引用)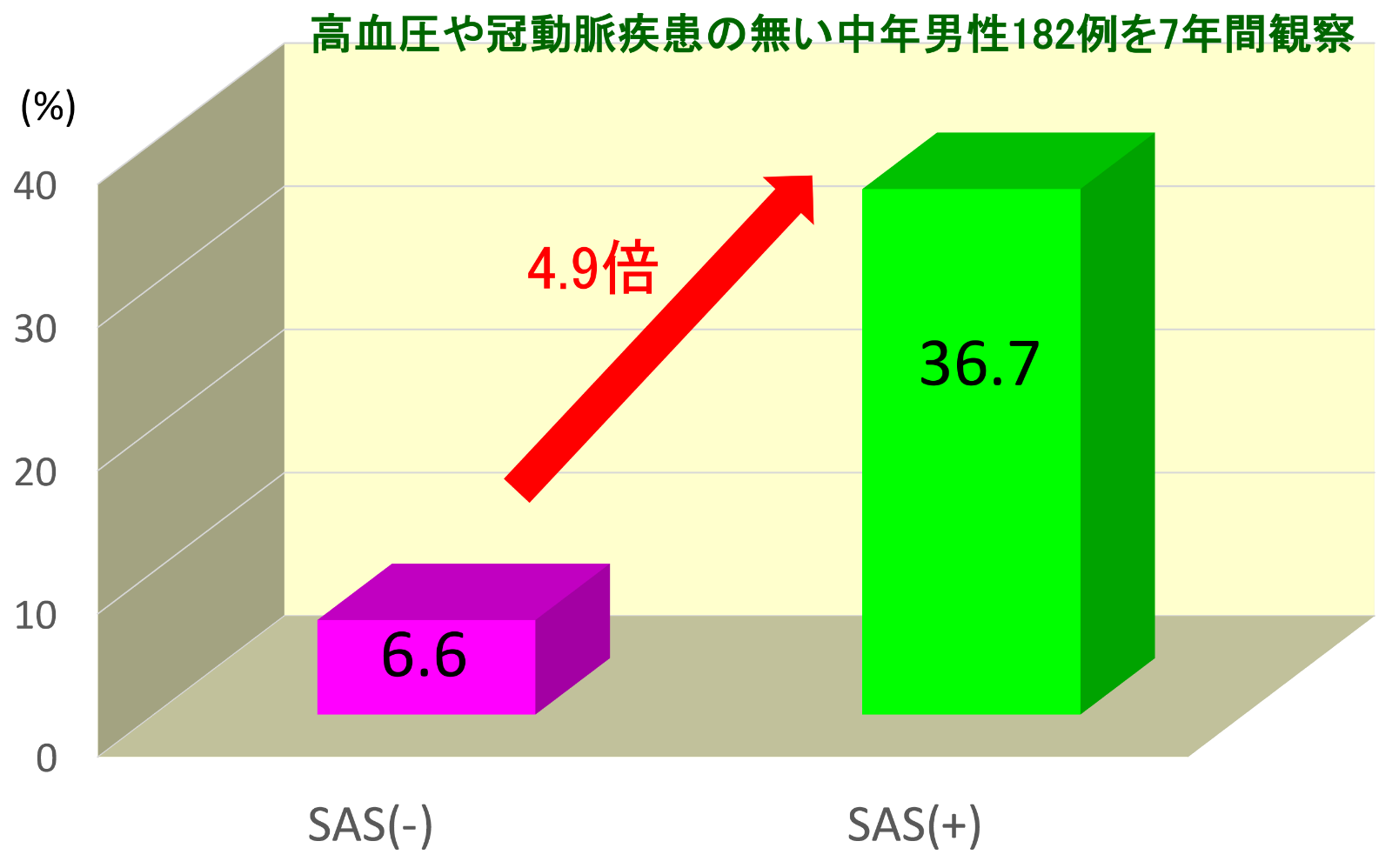
CSAでも無呼吸に伴う低酸素血症、肺伸展反射の消失、中途覚醒が交感神経活性を亢進させるとともに、一過性低酸素と再酸素化による影響が起こります。またCSAにおける呼吸努力の消失は正常な周期的胸腔内圧陰圧化を消失させ、引き続く過呼吸と共に静脈還流に影響を与えます。CSAは循環器疾患の中でも主に心不全などのより重篤な病態に合併するため、これらのメカニズムによる悪影響の度合いが弱くても、もともと悪い心機能は容易に悪影響を受けるものと考えられています。
心不全患者における睡眠呼吸障害の頻度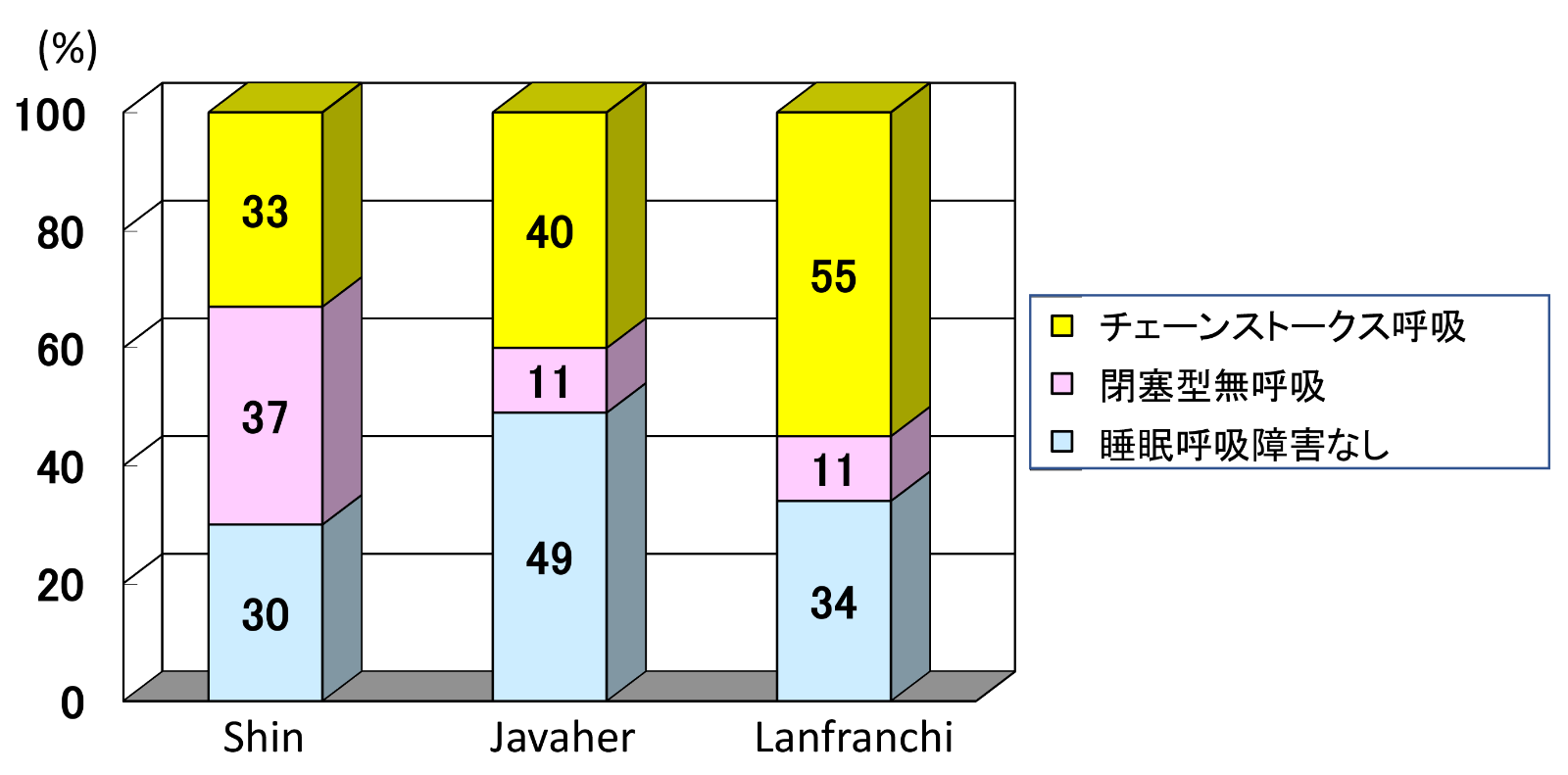
またSASのうち、特にOSAは脳卒中をはじめとした血管障害と強い関連があります。睡眠中の頻回の閉塞性呼吸イベントにより間欠的夜間低酸素血症と覚醒反応に伴う睡眠の分断化が生じ、脳卒中発症に関連する因子として、交感神経活動の活性化による高血圧や不整脈、血管内皮障害などの脳血管の反応性低下、炎症反応や酸化ストレスなどの動脈硬化を惹起する生体反応、代謝障害、血小板活性や血液凝固能の亢進などが起こります。これらが複合的に絡み合うことで大脳白質病変や頸動脈病変を引き起こして脳卒中発症の危険因子となります。
動脈血酸素飽和度95%未満の時間の割合による微小脳梗塞の発症率
(Gelber RP, et al. Neurology 2015より引用)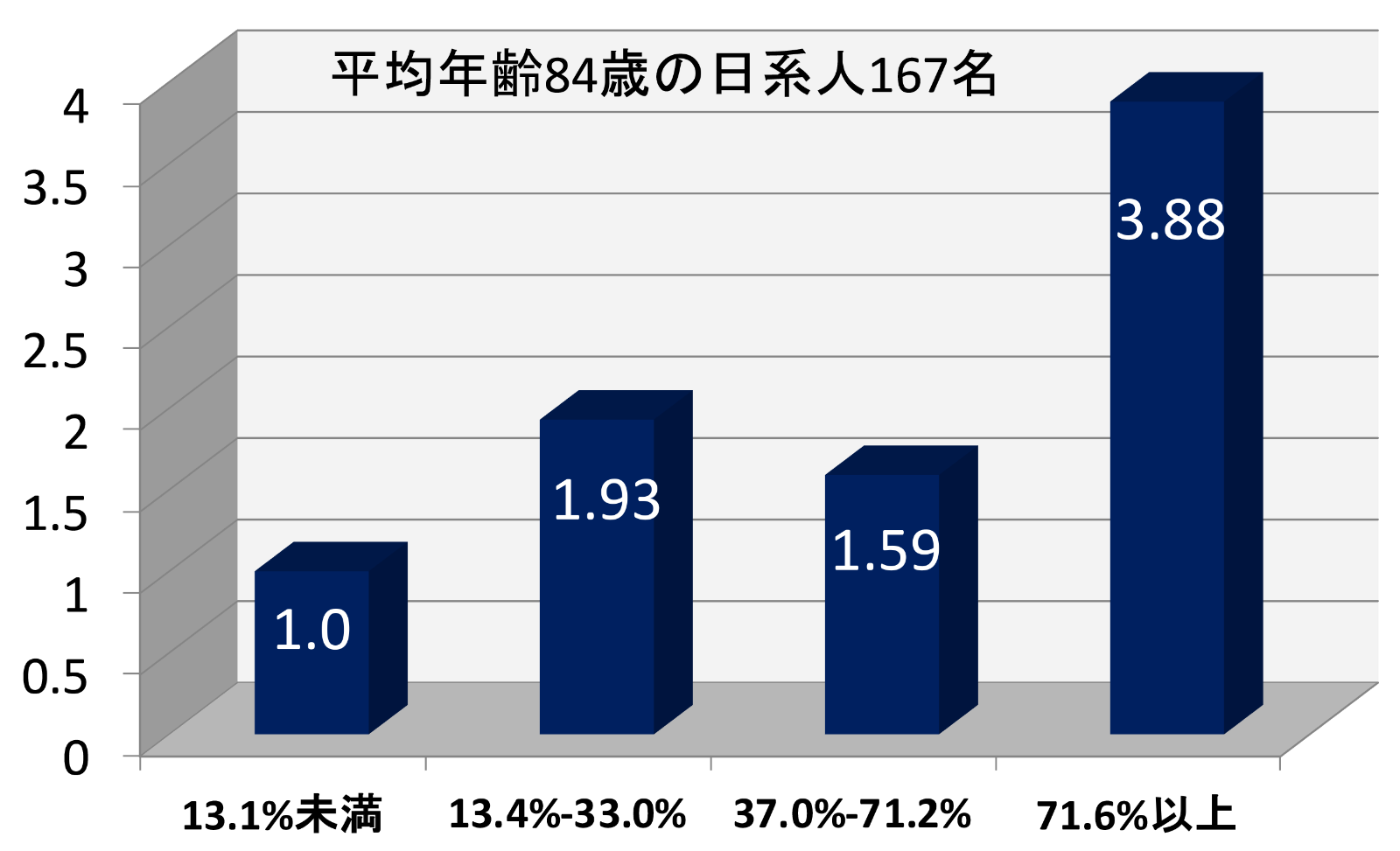
各種循環器疾患における睡眠時無呼吸症候群
1:冠動脈疾患(狭心症・心筋梗塞)
冠動脈疾患にOSAを合併する頻度は35%~40%であり、冠動脈疾患のない場合の約2倍の合併率です。急性冠症候群では更に高頻度にOSAが合併し、心機能障害に関連してCSAを認める症例もあります。OSAが冠動脈疾患発症の直接の原因となることは、OSAを合併する心筋梗塞では発症時間が午後10時から早朝6時の夜間帯のものが多くなることから裏付けられており、また海外で行われた大規模研究においてもOSAの程度と心筋梗塞や脳梗塞の発症頻度に強い相関がみられることや、無呼吸低呼吸指数が30以上の重症OSAではOSAのない患者に比べてイベント発症リスクが68%高くなることなどが報告されています。また、心筋梗塞を含む夜間の心臓突然死とOSAの関連も示唆されており、その機序には無呼吸低呼吸指数の重症度よりも血液の酸素飽和度低下との関連が示唆されています。急性心筋梗塞の発症には、全身血管の器質的障害や機能的障害を背景としながら、易血栓性が関与することが知られています。OSAでは、全身の血管障害を進行させることに加えて、血液凝固能を亢進させることによって心筋梗塞の発症に影響すると考えられています。
急性心筋梗塞の発症時間とSAS合併の有無との関係
(Kuniyoshi FH, et al. J Am Coll Cardiol 2008より引用)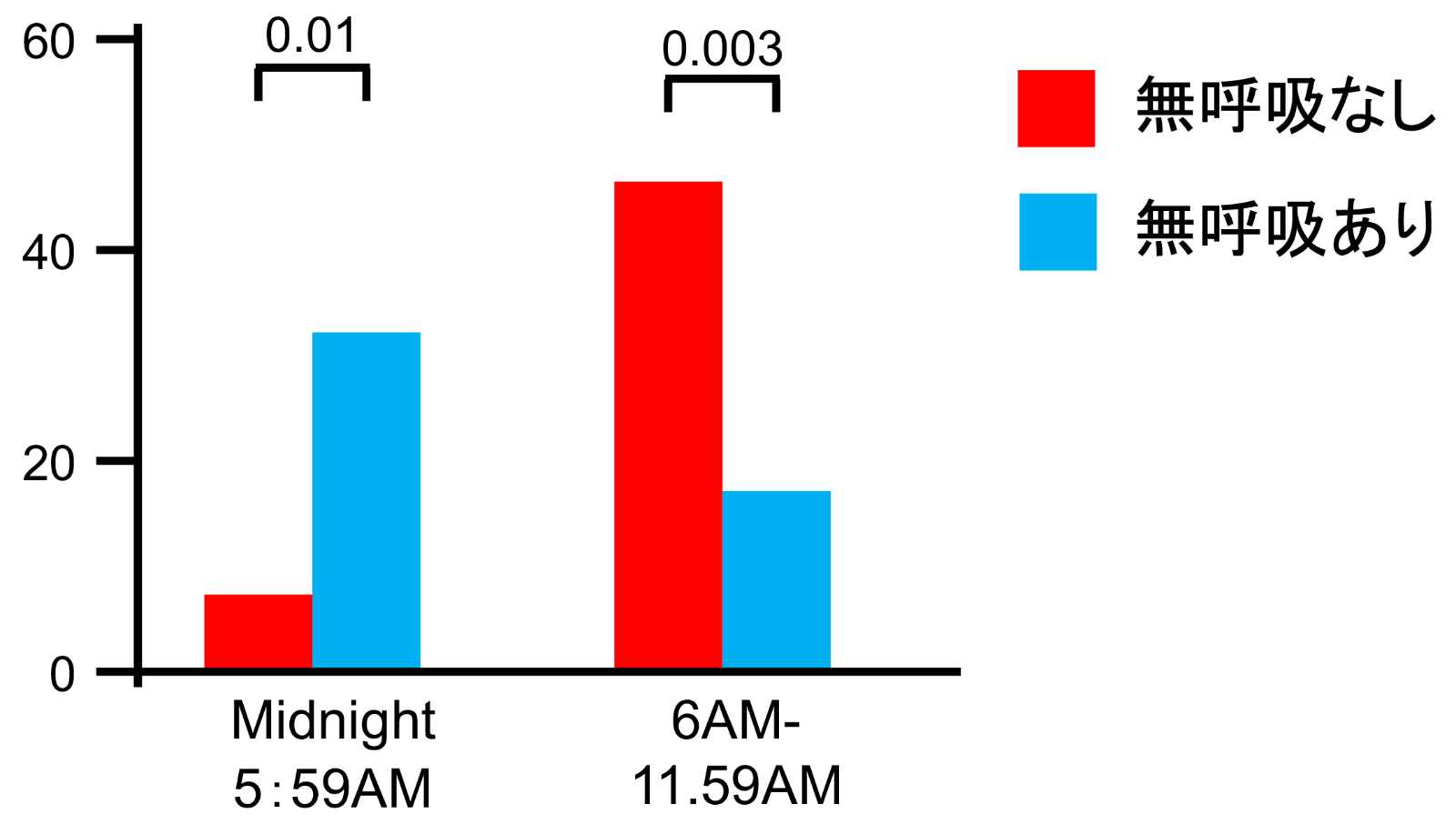
すでに冠動脈疾患を有する患者にOSAが合併すると心血管イベントの発症率は高くなりますが、これはカテーテルによる経皮的冠動脈インターベンション治療(PCI)が広く普及している現在においても同じです。PCIを受けたOSA患者390名を対象とした研究では、中等症~重症のOSAの無治療群はCPAP治療群と比べて血行再建術のリスクが2倍以上になることが報告されており、PCI後のCPAP治療は血行再建術のリスクを軽減することが示唆されます。
PCIを受けた患者の予後とSAS治療
(Cassar A, et al. J Am Coll Cardiol 2007より引用)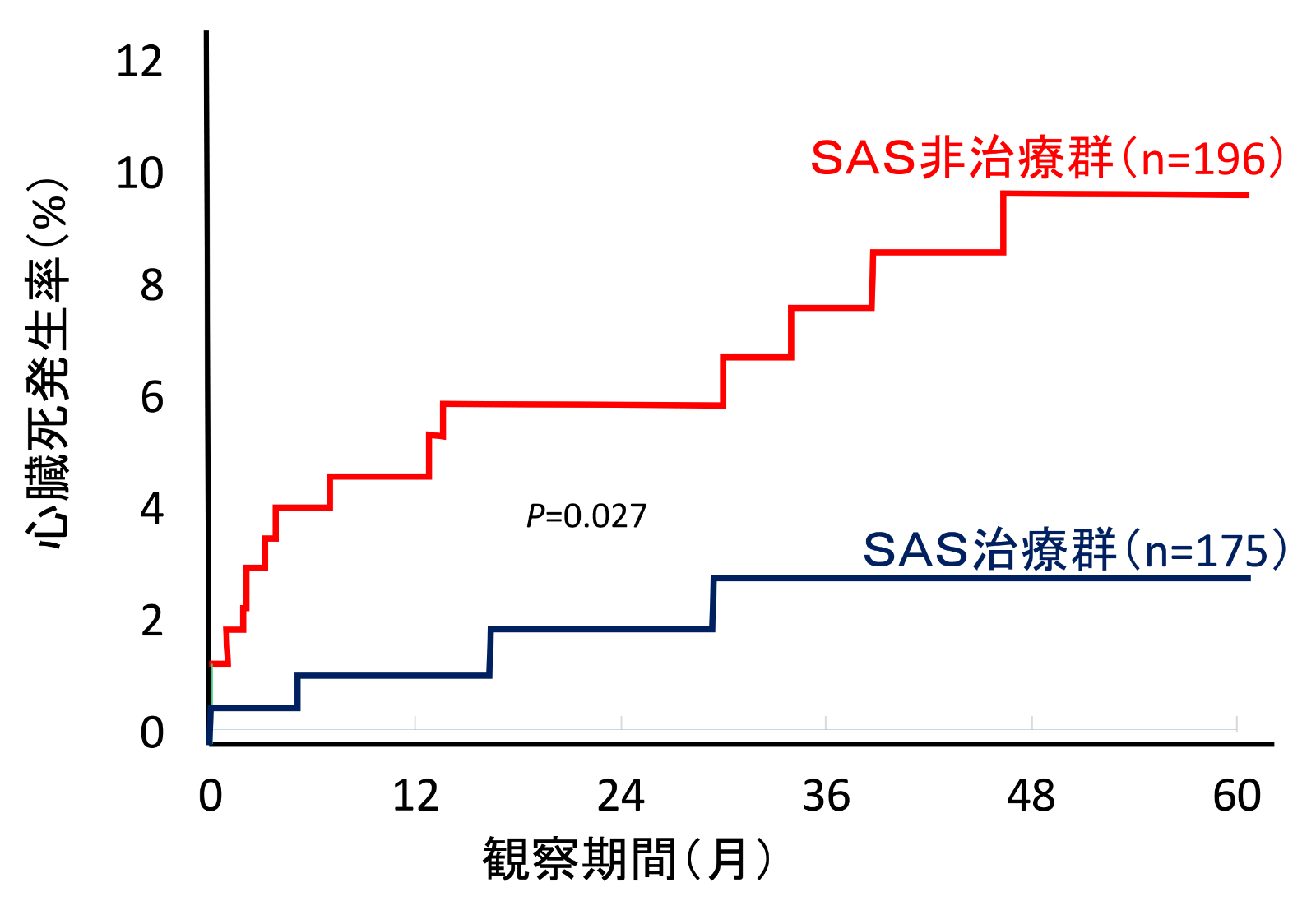
また、血行再建術後の眠気の自覚がない中等症~重症のOSA患者を対象としてCPAPの効果を調べた研究では、CPAPを1日に4時間以上使用した群は4時間未満もしくは無治療群に比べて心血管リスクが29%有意に減少したことが報告されており、CPAPの使用は1日に4時間以上が望ましいことが示唆されています。更には、心疾患を有さないSAS患者に対してCPAP治療を行うと心血管イベント発症率がSASを有さない人とほぼ同レベルまで低下することも報告されています。
CPAP治療による心血管病の抑制効果
(Marin JM, et al. Lancet 2005より引用改変)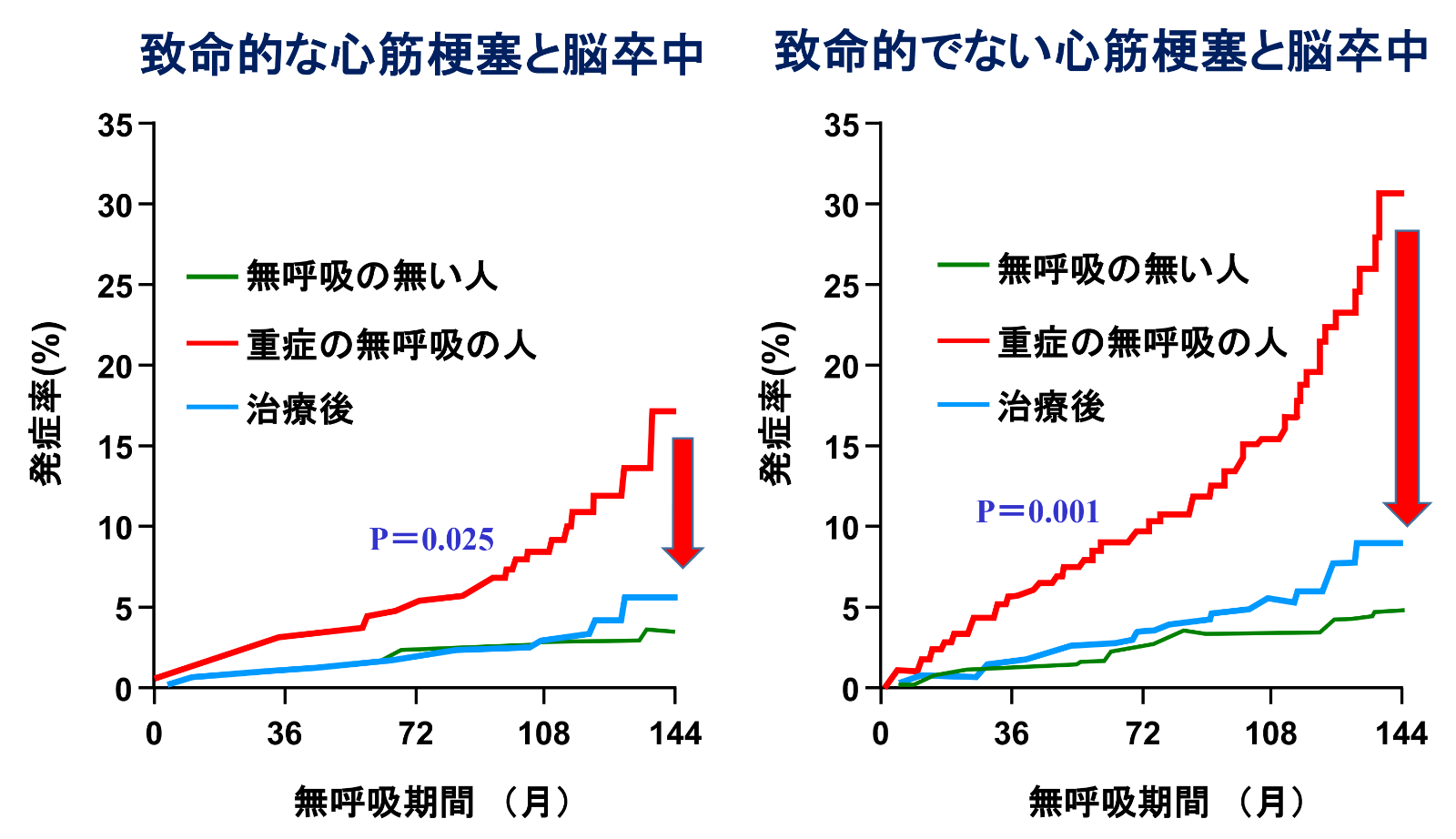
2:大動脈疾患
OSAでは、夜間呼吸イベントごとの交感神経活動の亢進と共に、胸腔内圧の高度陰圧化が周期的に生じることにより、睡眠時の血圧は周期的に急激な上昇と下降を繰り返しています。このような夜間高血圧は大動脈拡張、大動脈解離などの大動脈疾患の主要なリスクになります。一方、胸腔内圧の陰圧化も胸部大動脈壁を外側へ引っ張るような力がかかるため大動脈疾患のリスクになることが示唆されています。実臨床での検討においても、OSAを合併する群では合併しない群に比べてCTで調べた平均上行大動脈径が5.3mmも大きかったことが報告されており、高血圧のみならず繰り返しの無呼吸・低呼吸イベントによる機械的ストレスが大動脈拡大に関与することが示唆されています。また大動脈解離を発症した患者においても、対象群と比べて未診断の重症OSAの有病率が37%と高いのみならず、夜間睡眠中の酸素飽和度低下指数を指標とした再酸素化の割合が有意に高いことが報告されています。
OSA合併の有無による平均上行大動脈径の差
(McNamura SG, et al. Sleep and Breathing 1994より引用)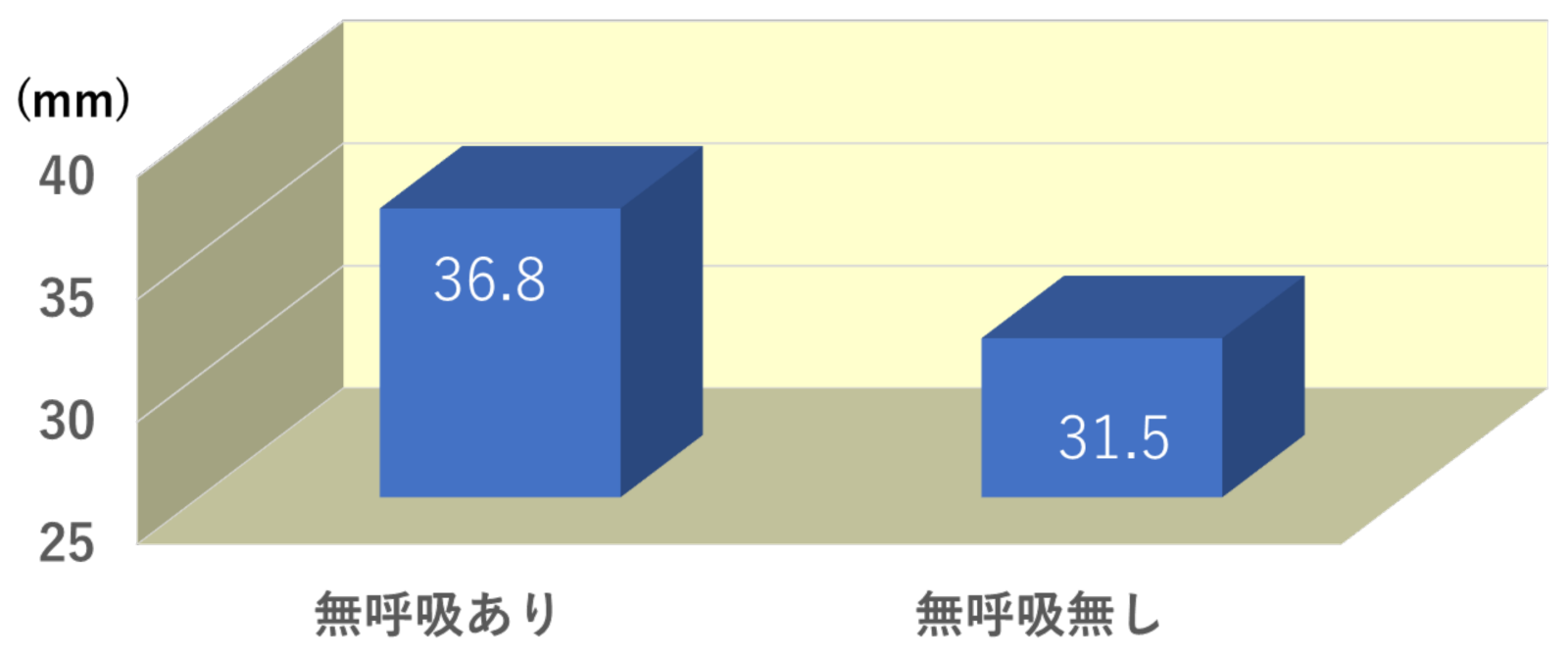
3:不整脈
OSA患者では無呼吸中の徐脈と呼吸再開時の頻脈を繰り返し、睡眠中では徐脈性不整脈と頻脈性不整脈のいずれも合併し、特に心房細動患者においては約50%にOSAが合併していることが報告されています。これらの不整脈は、無呼吸による低酸素血症及び呼吸性アシドーシス、交感神経活動の亢進などに伴い生じるものであり、時には致死的不整脈を来して突然死と関連する可能性が指摘されています。洞徐脈、洞停止、房室ブロックなどの徐脈性不整脈の合併はSASの約5%~10%ですが、頻脈性不整脈に関しては心房細動が重症SASの約5%にみられ、健常人の約5倍の合併リスクです。更には、心室性期外収縮の合併は25%で健常人の約2倍、非持続性心室頻拍の合併は約5%で健常人の約4倍のリスクであることも報告されています。また、OSA患者では、発作性心房細動、発作性上室性頻拍、心室性期外収取、非持続性心室頻拍のいずれもが睡眠と関連して出現し覚醒により軽減することも報告されています。
SASにおける不整脈の合併頻度
(Mehra R, et al. Am J Respir Crit Care Med 2006より引用)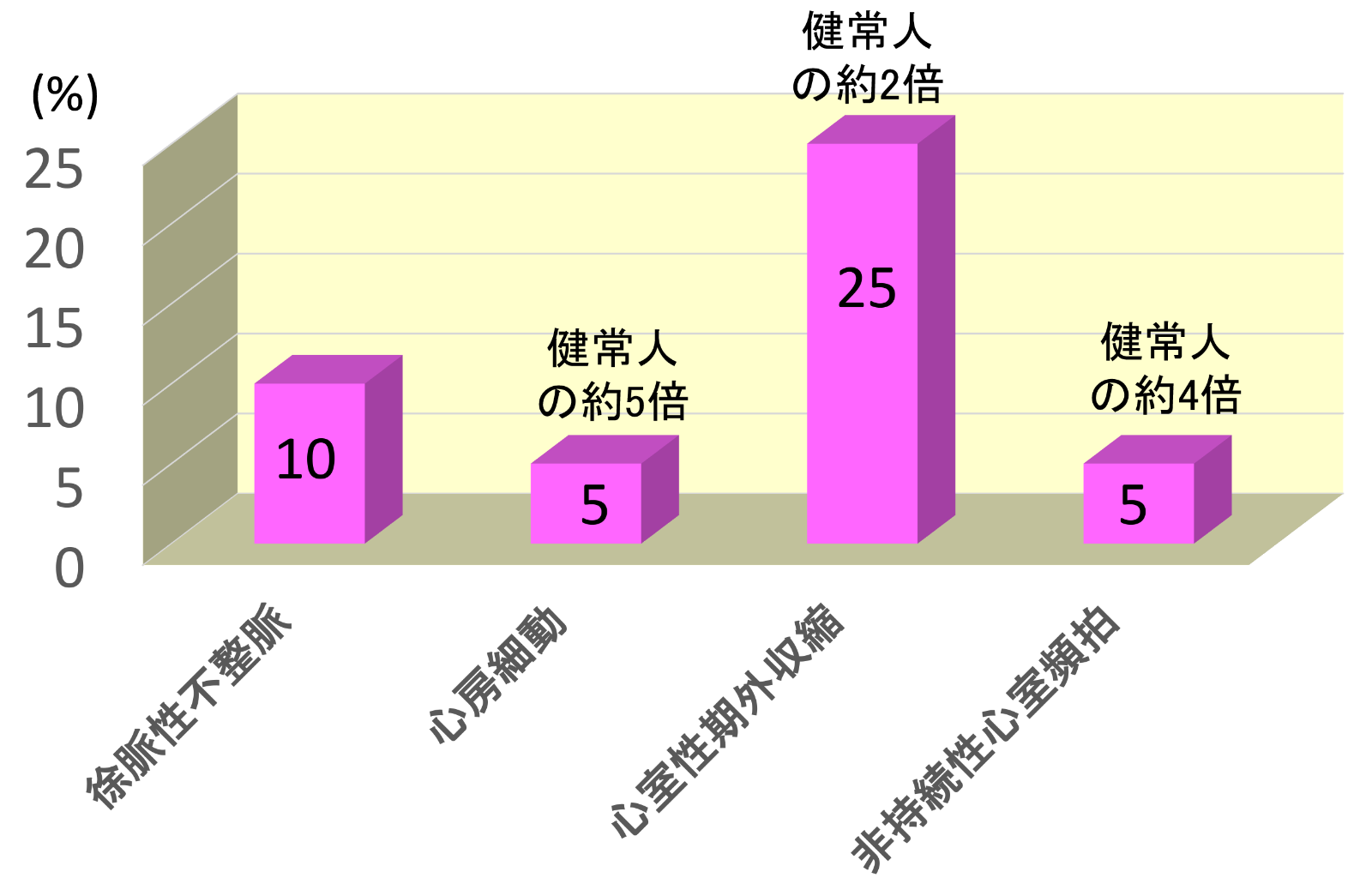
不整脈を有する患者においてもSASの合併は、その状態や予後を悪化させます。OSAの合併は心房細動患者の電気的除細動やカテーテルアブレーション後の再発リスクを上昇させることが知られており、心室性頻拍などに対して植込み型除細動器の植込みがなされている症例においてもOSAの合併により除細動ショックが与えられる可能性が高まることが知られています。一方で、OSAに対するCPAP治療によって不整脈発生が抑えられることも知られており、メタ解析の結果ではCPAP治療を受けたOSA患者は心房細動リスクが44%低下することが報告されています。また、心房細動の電気的除細動やカテーテルアブレーション後の再発に関しての報告でもCPAPによる再発抑制効果が認められています。例えば、OSAを合併する心房細動患者への電気的除細動後の心房細動再発率はCPAP治療群では42%であり、CPAP治療をしなかった群の82%に比べ有意に低かったことや、カテーテルアブレーション後のOSA患者の心房細動非再発率はCPAP治療群で71.9%であり、CPAP治療をしなかった群の36.7%と比べて有意に高いことなどが報告されています。また、CPAPによるOSA治療によって交感神経活性の低下に伴い心室性期外収縮の頻度が減少したことも報告されています。
カテーテルアブレーション後の心房細動再発率
(Naruse Y, et al. Heart Rhythm 2013より引用)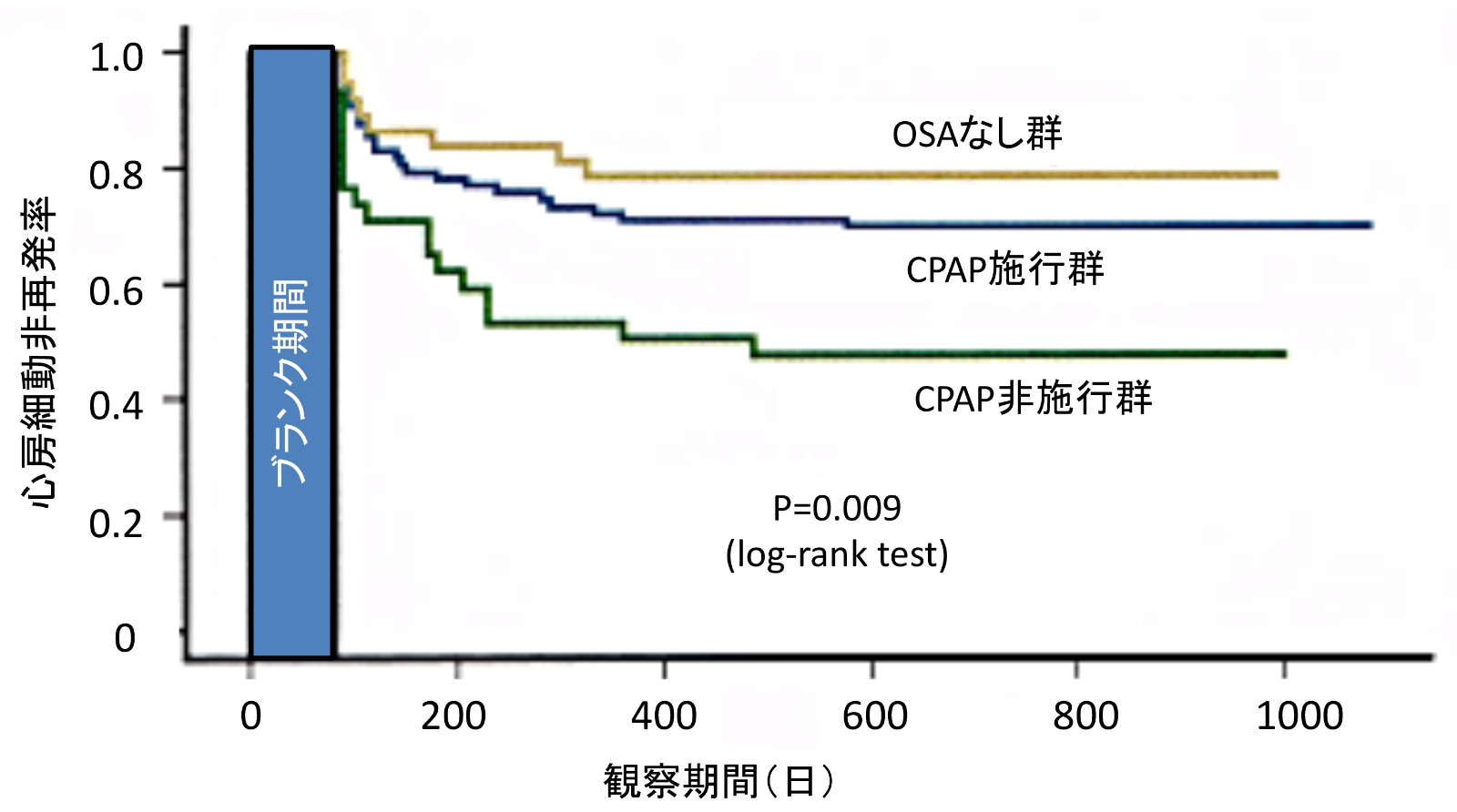
4:心不全
心不全の50%~80%にSASを合併するとされていますが、その特徴はOSAに加えてCSAの合併が多いことです。標準的な薬物治療を行っても労作時呼吸苦の症状を呈する心機能が低下した心不全患者700名を調査した報告においても、無呼吸・低呼吸指数が15以上のOSAは19%、CSAは33%に認められました。米国の一般住民における横断研究ではOSAがあると約2.4倍心不全を合併しやすく、また心不全にOSAが合併した場合の予後は不良であることも報告されています。これらは、OSAに伴う一過性低酸素血症、交感神経活性亢進、上気道閉塞に対する吸気性努力によって起こる胸腔内の陰圧負荷などが血管系へ悪影響を及ぼすことによるものと考えられます。すなわち、OSAがあると心血管系へ悪影響を及ぼして心不全の原因となり、心不全発症後も存在するOSAは心不全状態を更に悪化させることになります。
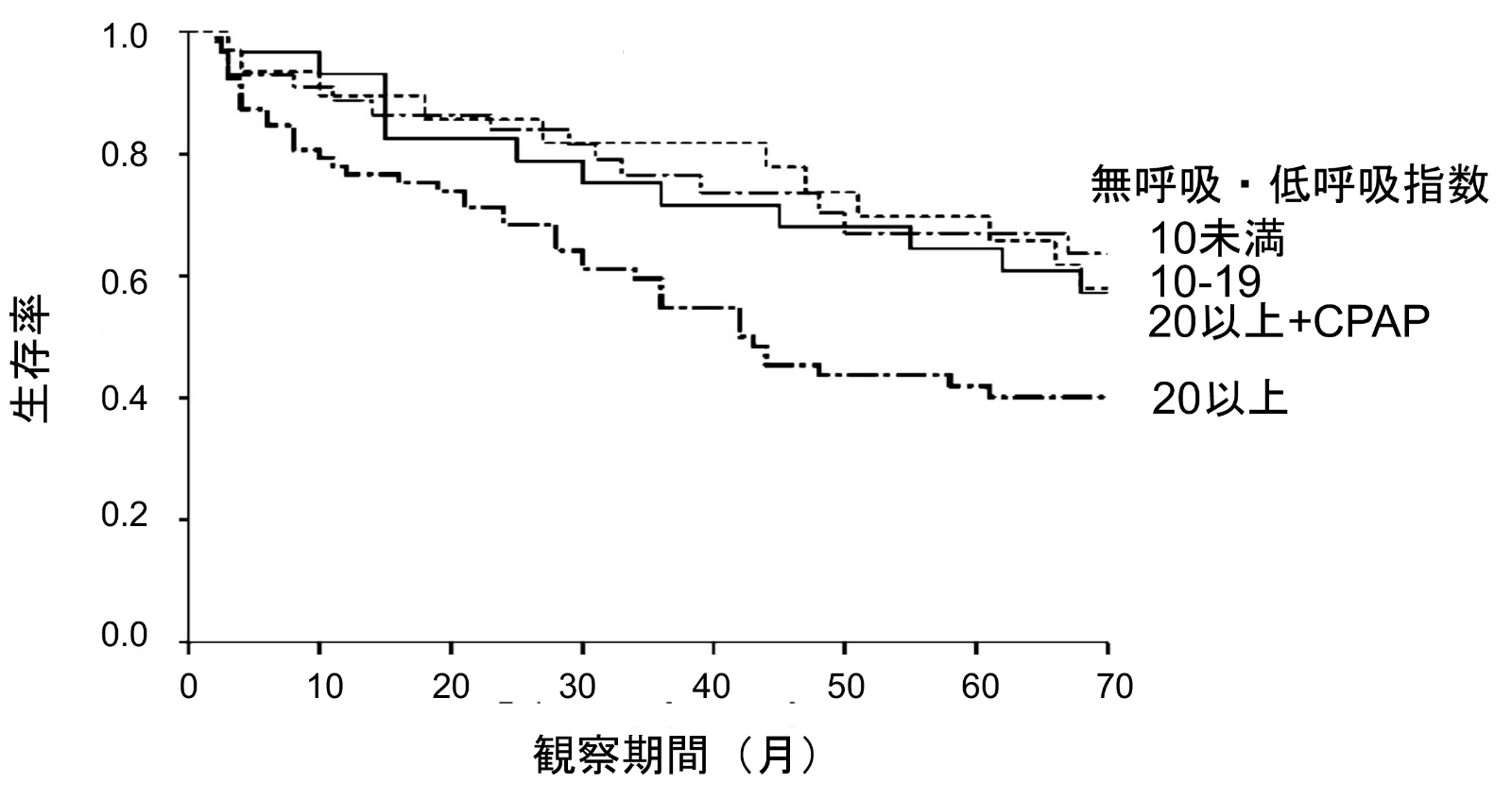
未治療OSAを合併した心不全患者の生存率
(Wang H, et al. J Am Coll Cardiol 2007より引用)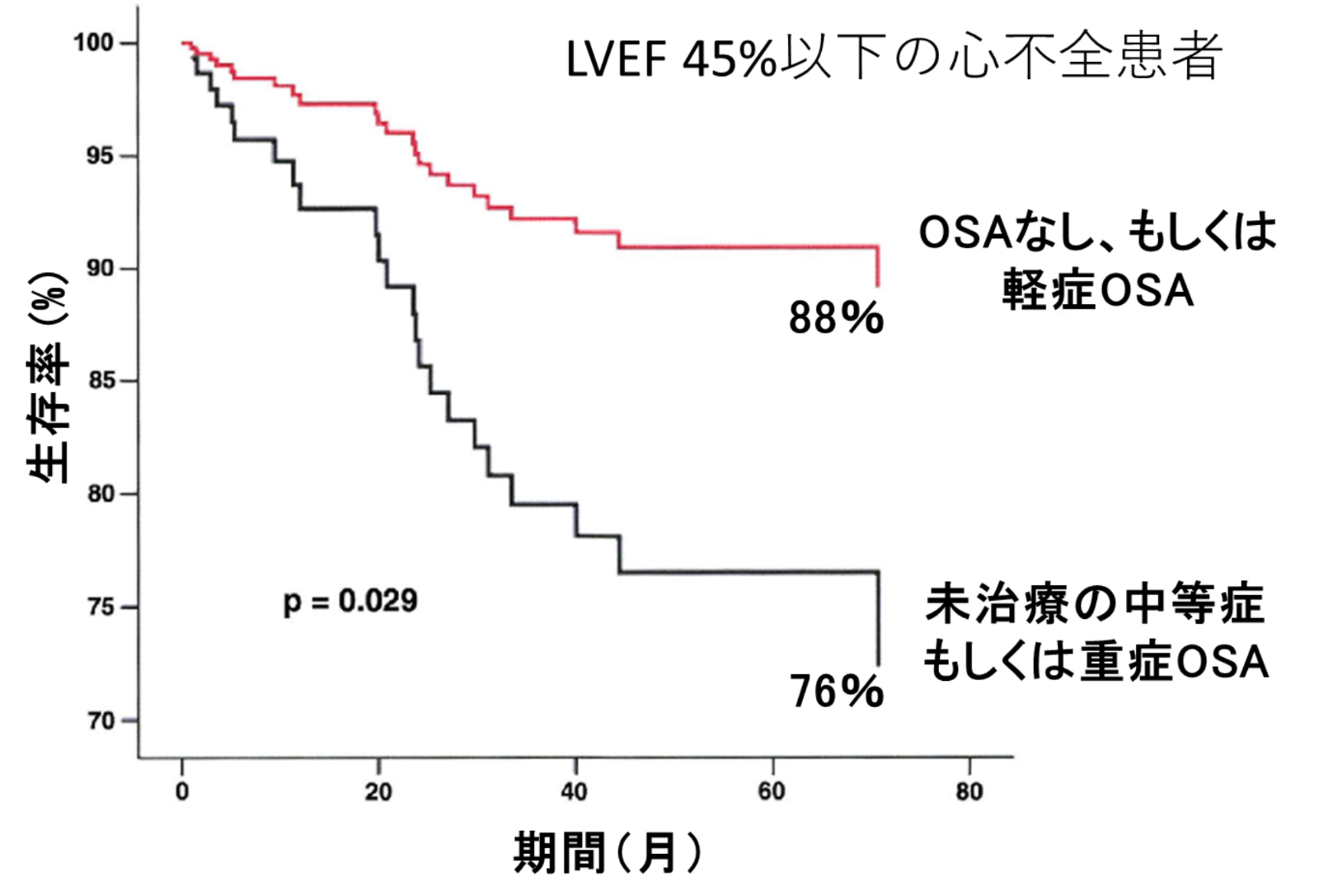
CSA発症の機序は肺うっ血による過呼吸刺激に伴う低炭酸ガス血症、化学受容体感受性亢進、心機能障害に伴う循環時間の延長とそれに伴う動脈血ガスの情報伝達の遅延、睡眠及び覚醒による無呼吸閾値の変動などの要因が挙げられます。つまり、CSAは心不全そのものが原因となるものであり、OSAとの関連においても、OSAから心不全を発症してCSAとなっている症例も存在すると考えられます。更には、左心室の収縮不全を呈する心不全患者ではCSAの合併は主要な予後予測不良に関連する因子であり、死亡リスクを約2.1倍上昇させるといわれています。なお、慢性心不全患者を対象とした観察研究において、CPAP治療が予後改善と関連することが報告されています。
OSA合併心不全患者におけるCPAPの予後改善効果
(Kasai T, et al. Chest 2008より引用)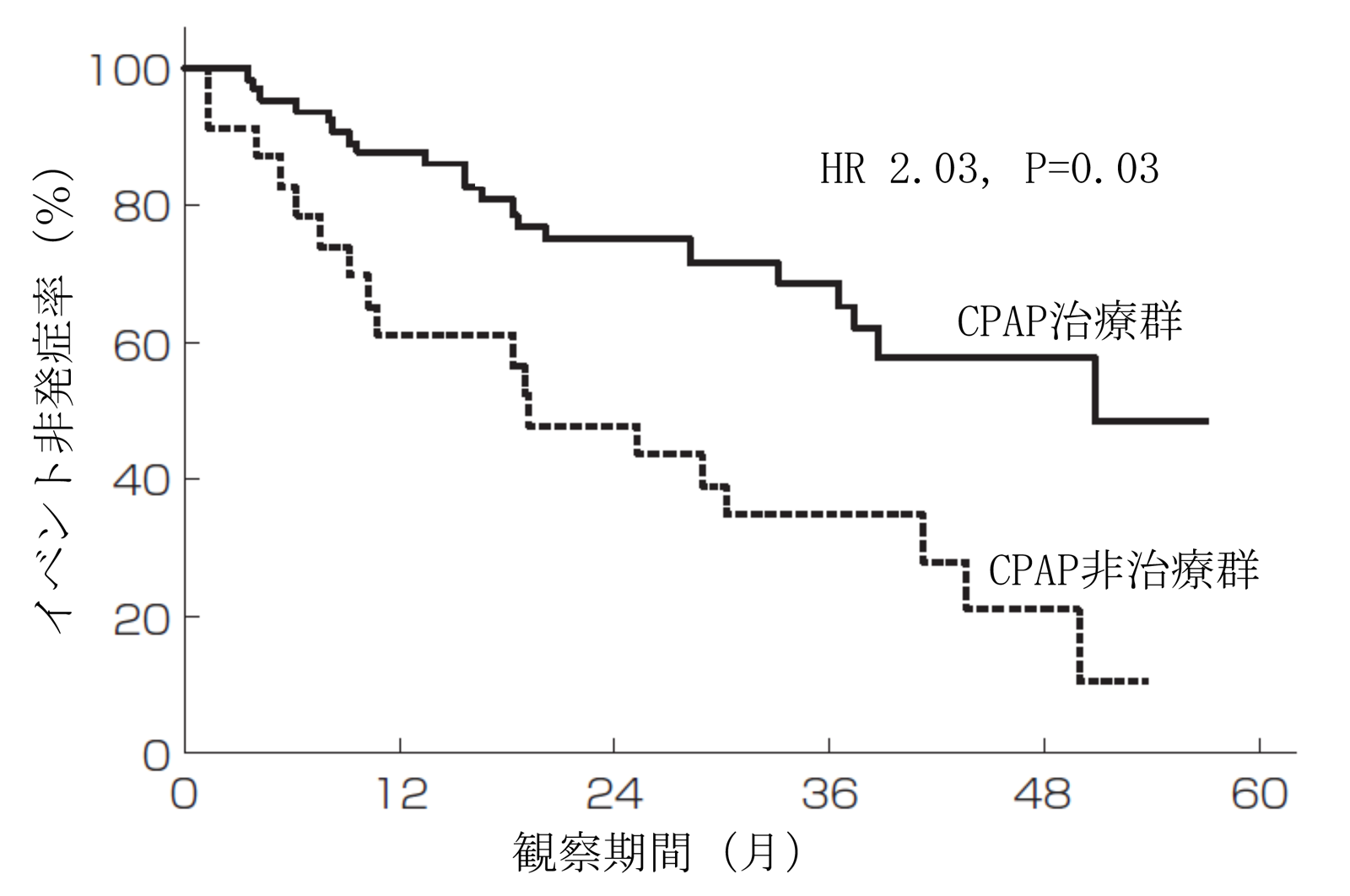
5:脳血管疾患
SASは心血管疾患とともに脳血管疾患に対してもリスク因子であることが知られており、無呼吸・低呼吸指数が15以上の中等症~重症のOSA患者における脳卒中発症リスクは健常人の約3.6倍になることやCSAも脳梗塞のリスクになることなども報告されています。海外で行われた29論文2,343例の脳梗塞患者のメタ解析の結果では、無呼吸・低呼吸指数が5以上の睡眠呼吸障害を有する患者の割合は72%で、無呼吸・低呼吸指数が30以上の重症SASを有する患者の割合は29%であったことが報告されています。また、本邦で行われた研究では無症候性脳梗塞は中等症以上のSASに多いことも報告されています。脳出血の有病率についての研究においても、無呼吸・低呼吸指数が5以上の睡眠呼吸障害を有する患者の割合は78.1%で、無呼吸・低呼吸指数が30以上の重症SASを有する患者の割合は28.1%であったことが報告されており、同時にSASは脳出血周囲の脳浮腫の程度に影響を与えることも明らかにされています。更には、本邦で行われた研究において、脳動脈瘤患者の88.2%にSASを認め、中等症以上のSASの割合は42%で、破裂例と未破裂例の重症度には差がなかったことも報告されています。
SAS合併による脳卒中の発症リスク
(Valham F, et al. Circulation 2008より引用)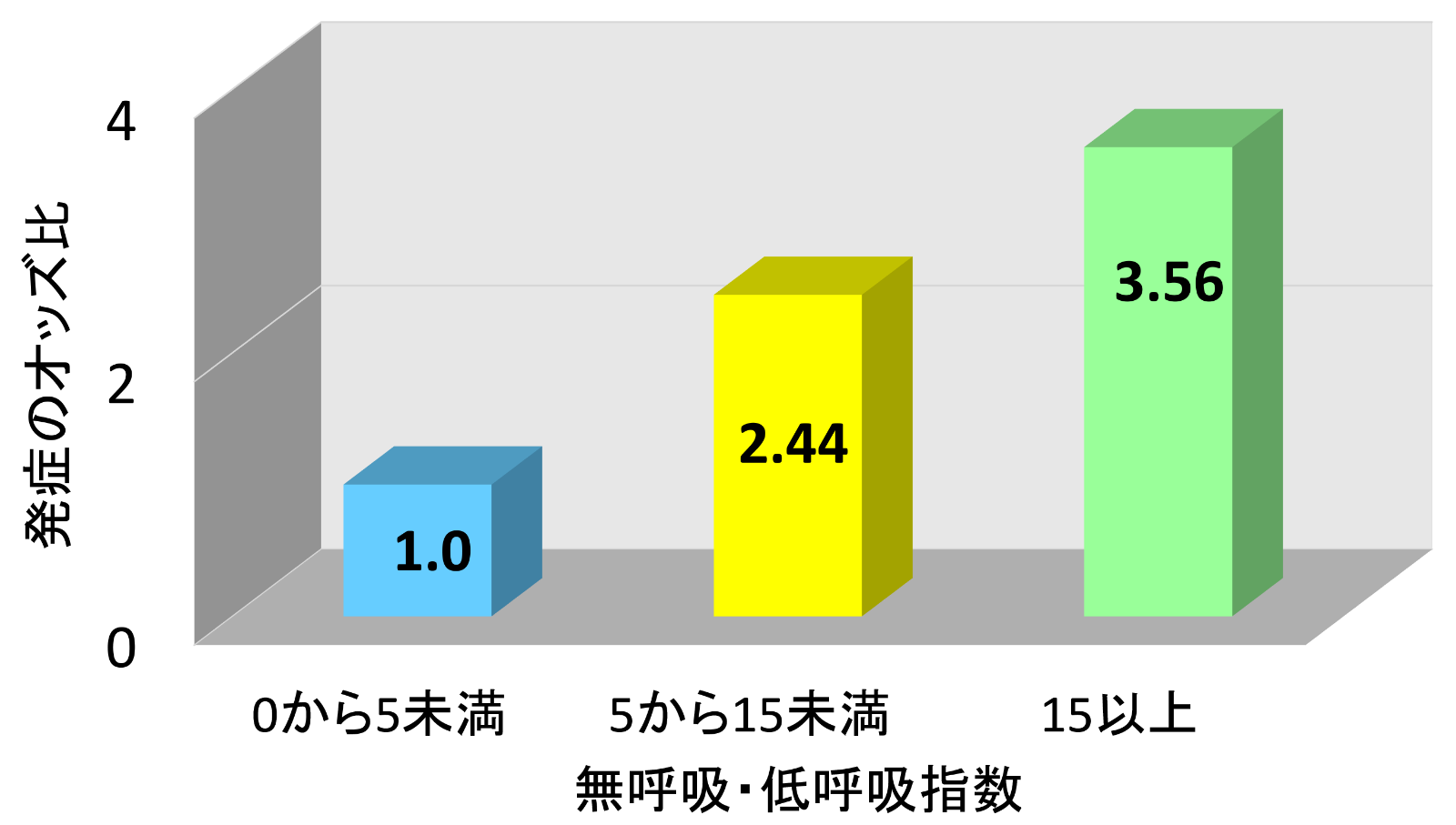
急性期脳梗塞に対するCPAP治療の効果を調べた研究では、脳梗塞発症後3日~6日でCPAP療法を開始することで1か月後の生活自立度スコア(modified Rankin Scale)と神経学的重症度(カナダ神経スケール)が改善することや、脳梗塞発症初日からCPAP療法を1日に4時間以上行うことで発症Ⅰ週間後の予後が改善することなどが報告されています。また慢性期においても、無呼吸・低呼吸指数が10以上のSASを合併していると脳卒中の再発リスクが3.5倍になることも報告されています。
脳梗塞後にOSAの治療をしないと予後不良
(Martnez-Garcia MA, et al. Am J Respir Crit Care Med 2009より引用)