『非アルコール性脂肪性肝疾患とは』
従来、慢性肝疾患の主な原因はウィルス性肝炎でしたが、現在では抗ウィルス薬の進歩などによりウィルス性肝炎は急速に克服されつつあります。一方で、食習慣を含めたライフスタイルの変化による肥満人口の急激な増加に伴い、全世界的に非アルコール性脂肪性肝疾患(NAFLD: non-alcoholic fatty liver disease)が急増しています。本邦においてもメタボリックシンドロームの患者数と共にNAFLDの患者数も増加しており、更にはNAFLDを背景とした肝臓癌の割合も着実に増加しています。
NAFLDの性・年齢別頻度
(Eguchi Y, et al. J Gastroenterol 2012より引用)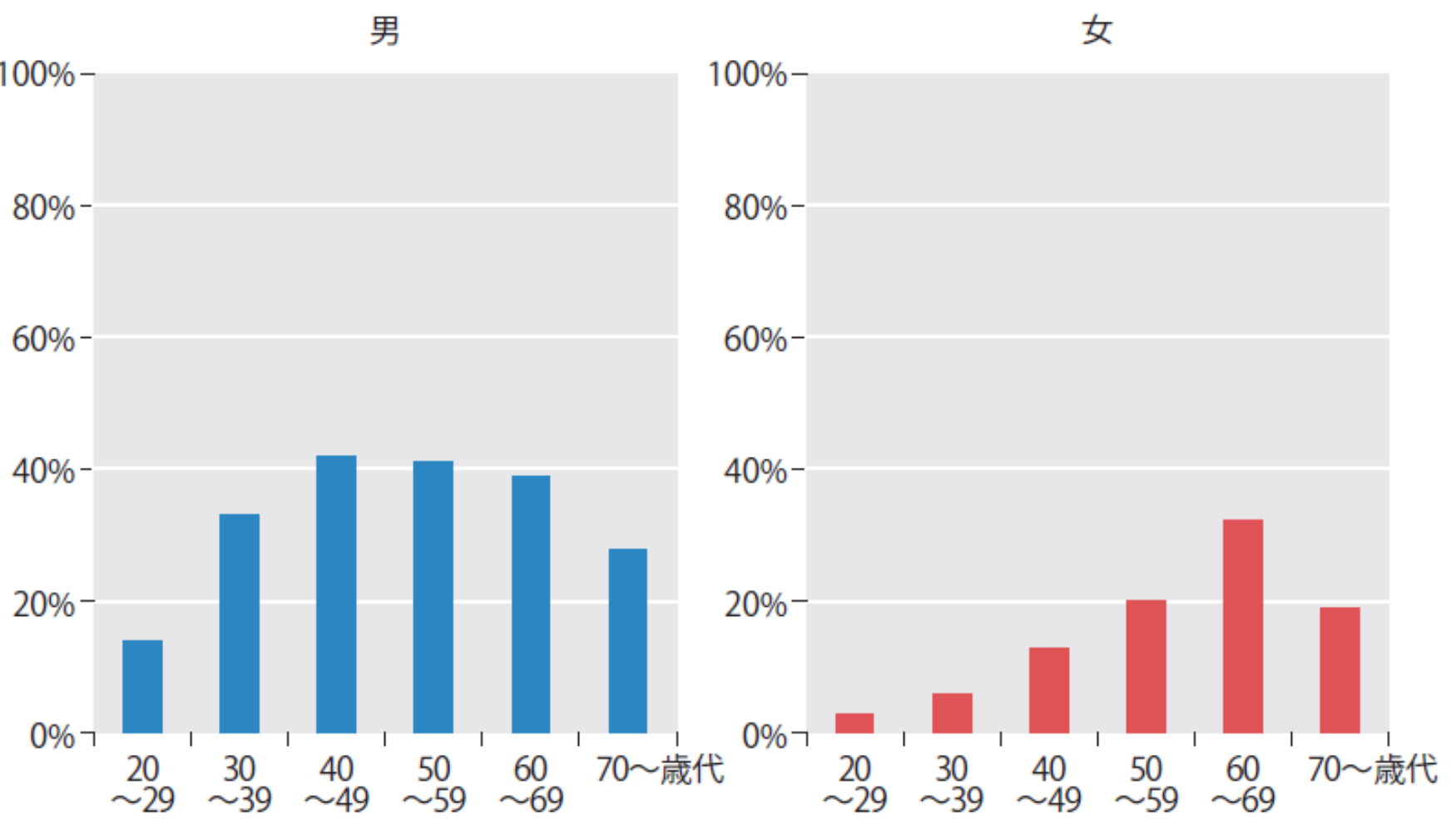
『非アルコール性脂肪性肝疾患の原因』
NAFLDとは、内臓肥満やインスリン抵抗性を主たる基盤として発症する病態で、肝組織診断あるいは画像診断において脂肪肝を認め、アルコール性肝障害や薬剤性肝障害などの他の肝疾患が除外できる疾患と定義されています。なお、エタノール換算で男性30g/日、女性20g/日以上の飲酒でアルコール性肝障害を発症し得るため、非アルコール性と定義される飲酒量としては、この量以下とされています。女性では女性ホルモン(エストロゲン)の影響により、少量の飲酒でアルコール性肝障害をきたしやすいため、飲酒量上限に性差が設けられています。エタノール換算量がほぼ20g/日に相当する健康的飲酒量は、ウィスキーダブル1杯、ビール中瓶1本、日本酒1合、ワイングラス2杯ですが、アルコール性肝障害を来たす飲酒量には個人差が大きいことが知られています。
『非アルコール性脂肪性肝疾患の症状』
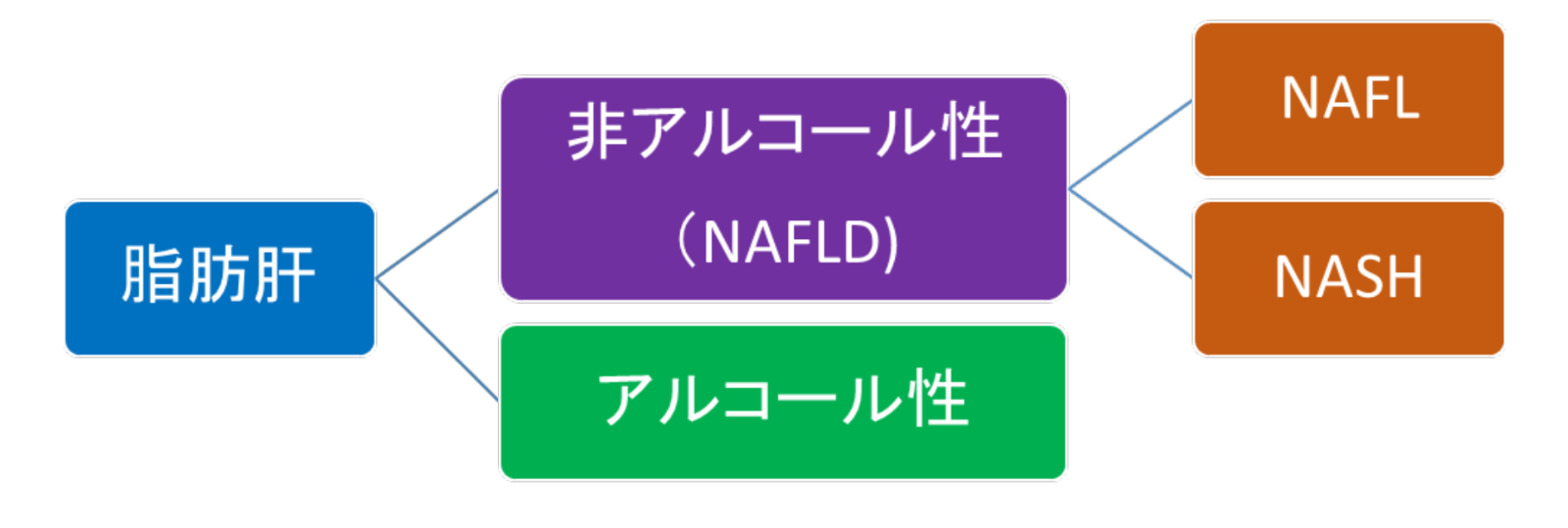
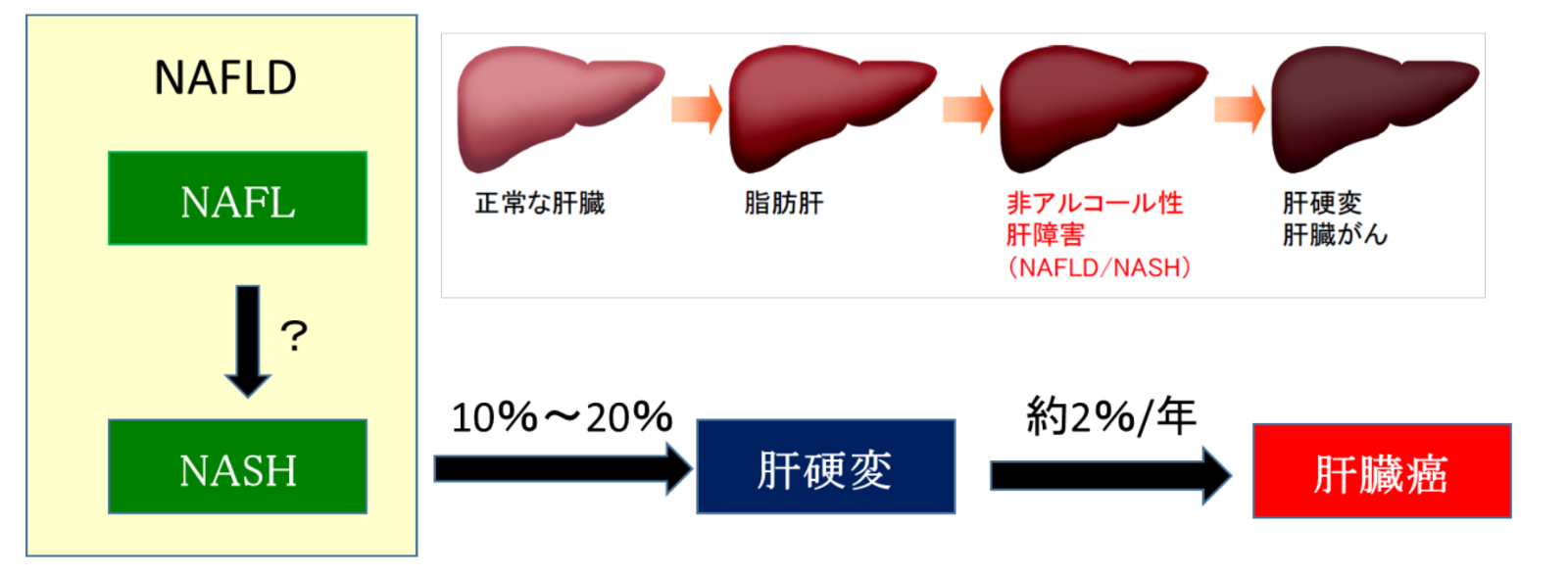
NAFLDは、組織学的に、肝細胞の脂肪変性を主体とする非進行性の非アルコール性脂肪肝(NAFL: non-alcoholic fatty liver)と、肝細胞の脂肪変性に加えて炎症や肝細胞の風船様変性、繊維化を呈して肝硬変や肝臓癌に進行し得る非アルコール性脂肪肝炎(NASH: non-alcoholic steatohepatitis)に分類され、後者が約10%~20%程度とされてきましたが、NAFLからNASHへの病態の移行を認めることから、近年、両者は移行し得る同一病態の別時相と考えられています。なお、NAFLDの診断は画像診断、NASHの確定診断は肝生検での組織診断により行われ、画像検査としては病状により腹部超音波検査、腹部CT検査、MRエラストグラフィー、フィブロスキャンなどが用いられます。採血ではNAFLDに特異的な検査はありませんが、肝臓の繊維化の有無の評価は、NAFICスコアやFib-4 indexなどの採血結果を組み合わせたスコアリングシステムを用いて行われます。
NAFLDの肝組織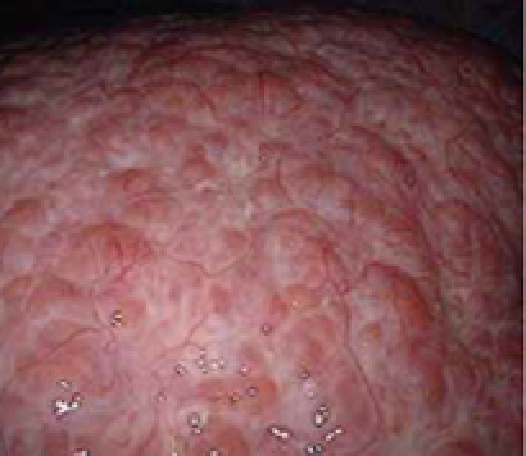
NAFICスコア
2点以上ならNASHの可能性が高い
NAFLからNASHや肝硬変への進展においては、肝臓への異所性脂肪蓄積から生じるインスリン抵抗性や自然免疫の過剰応答による炎症、細胞内ストレスを伴う肝臓の脂肪毒性などが共通のメカニズムと考えられていますが、なかでもインスリン抵抗性はNASHの成因において中心的な役割を果たしています。NAFLD患者の予後の規定因子としては、NASHであるかどうかよりも肝臓の繊維化があるかどうかのほうが重要であり、繊維化を伴わないNAFLDの15年生存率が70%~80%であるのに対して、繊維化を伴うNAFLDの15年生存率は60%であることが報告されています。
NAFLとNASHの肝疾患関連死亡率の比較
(McPherson S, et al. J Hepatol 2015より引用)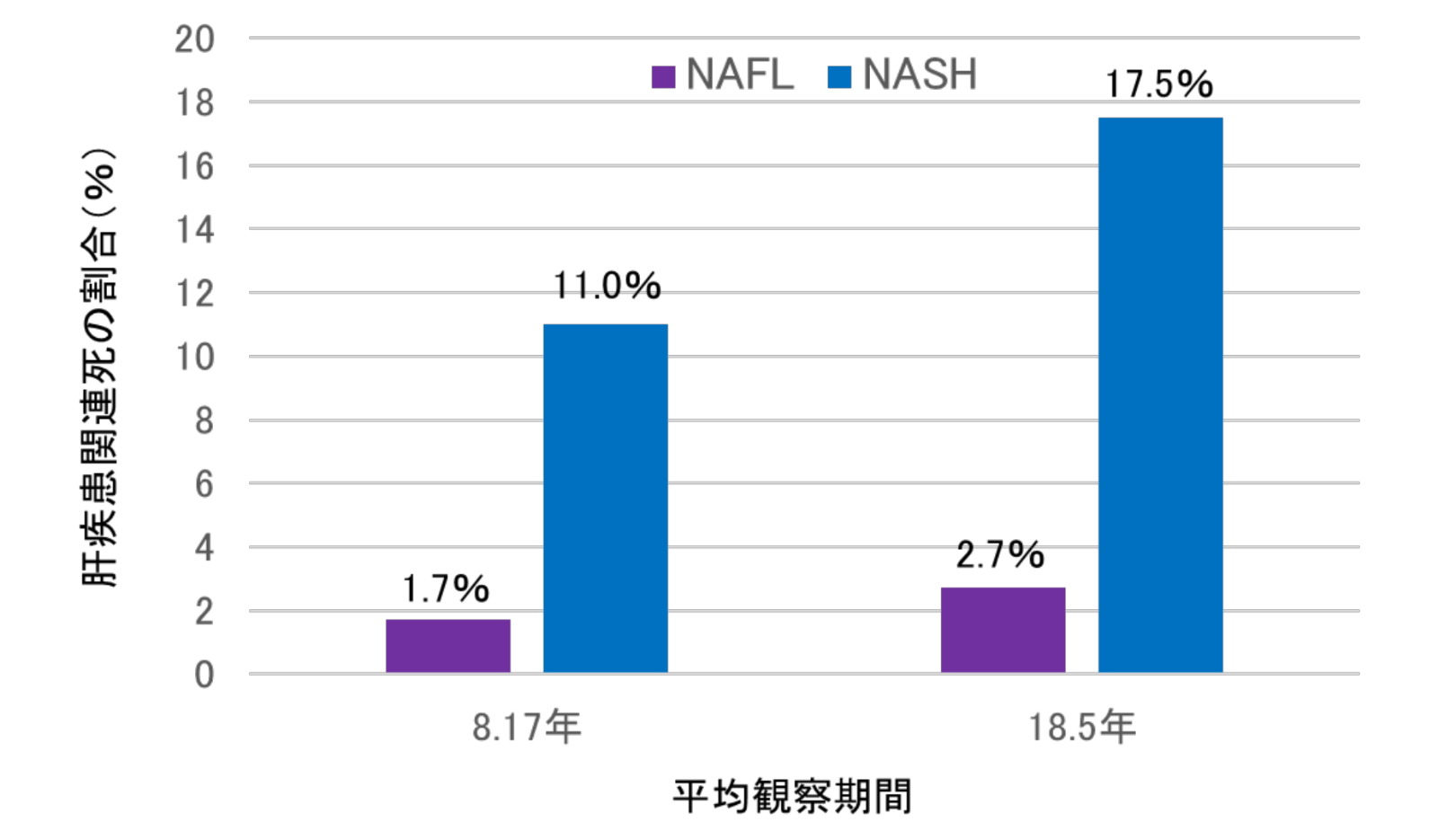
また、肝臓の繊維化は、心臓の拡張不全や心筋のグルコース取り込み障害とも有意に相関しており、肝臓の繊維化が心血管疾患や心不全の大きなリスク因子であることも明らかになっています。そのため、繊維化の抑止はNAFLD/NASHの治療標的として最も重要と考えられています。NAFLDにおける肝臓の繊維化の経過についての研究の結果では、3.2年~13.8年の経過で、32%~53%で繊維化が悪化、30%~50%で不変、16%~29%で繊維化が改善したと報告されています。
肝生検を施行したNAFLDの組織学的変化
(Kawanaka M, et al. Hepatology 2017より引用)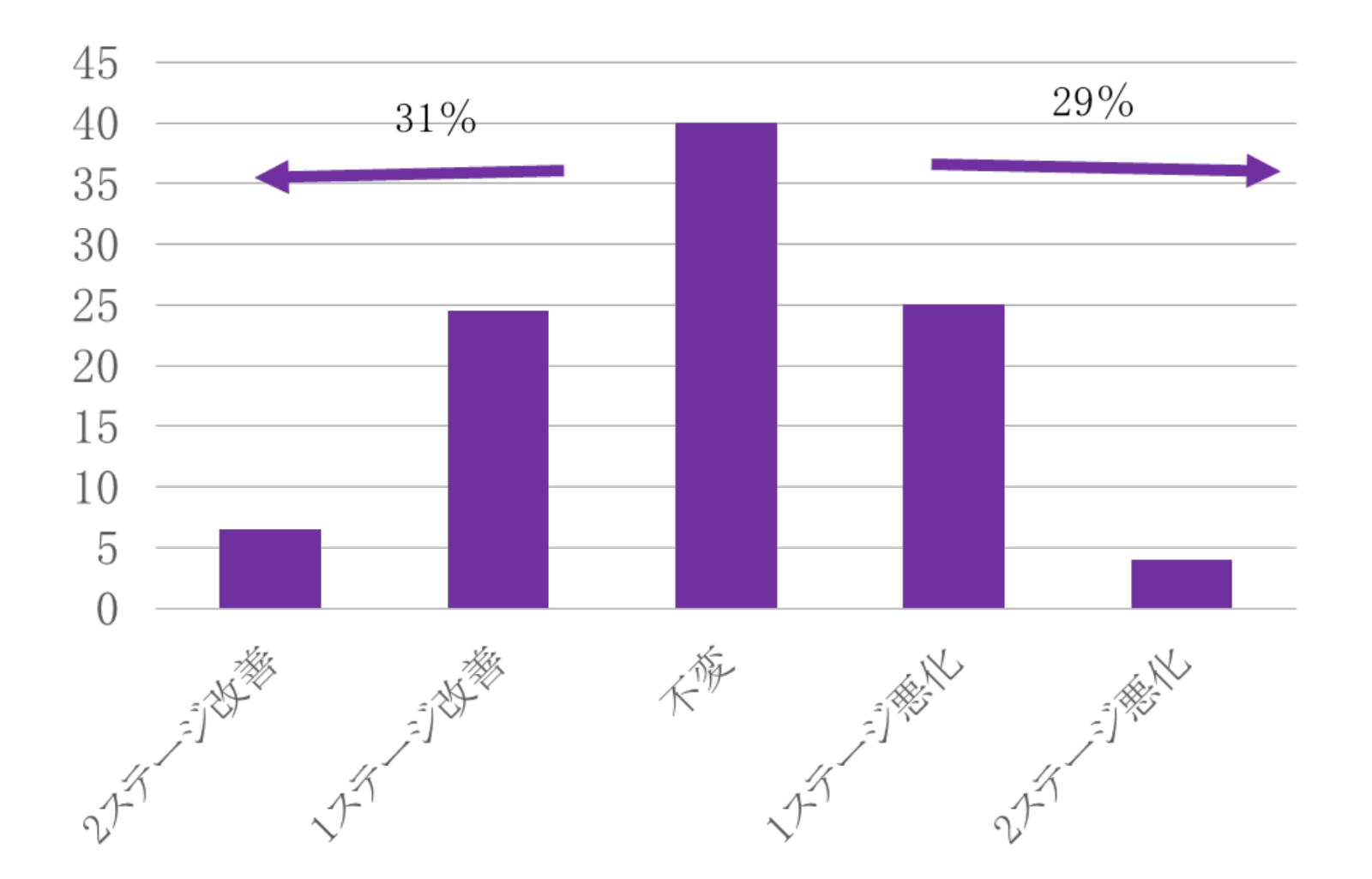
NAFLDの肝予後について調べた研究の結果では、NAFLD全体からは8年~21年の経過で5%~8%が、NASHからは5年~10年の経過で10%~20%が肝硬変に進行し、肝硬変症例からは年率約2%の頻度で肝臓癌を呈することが報告されています。
5年後の肝細胞癌の発癌率
(Yatsuji S, et al. J Gastroenterol Hepatol 2009より引用)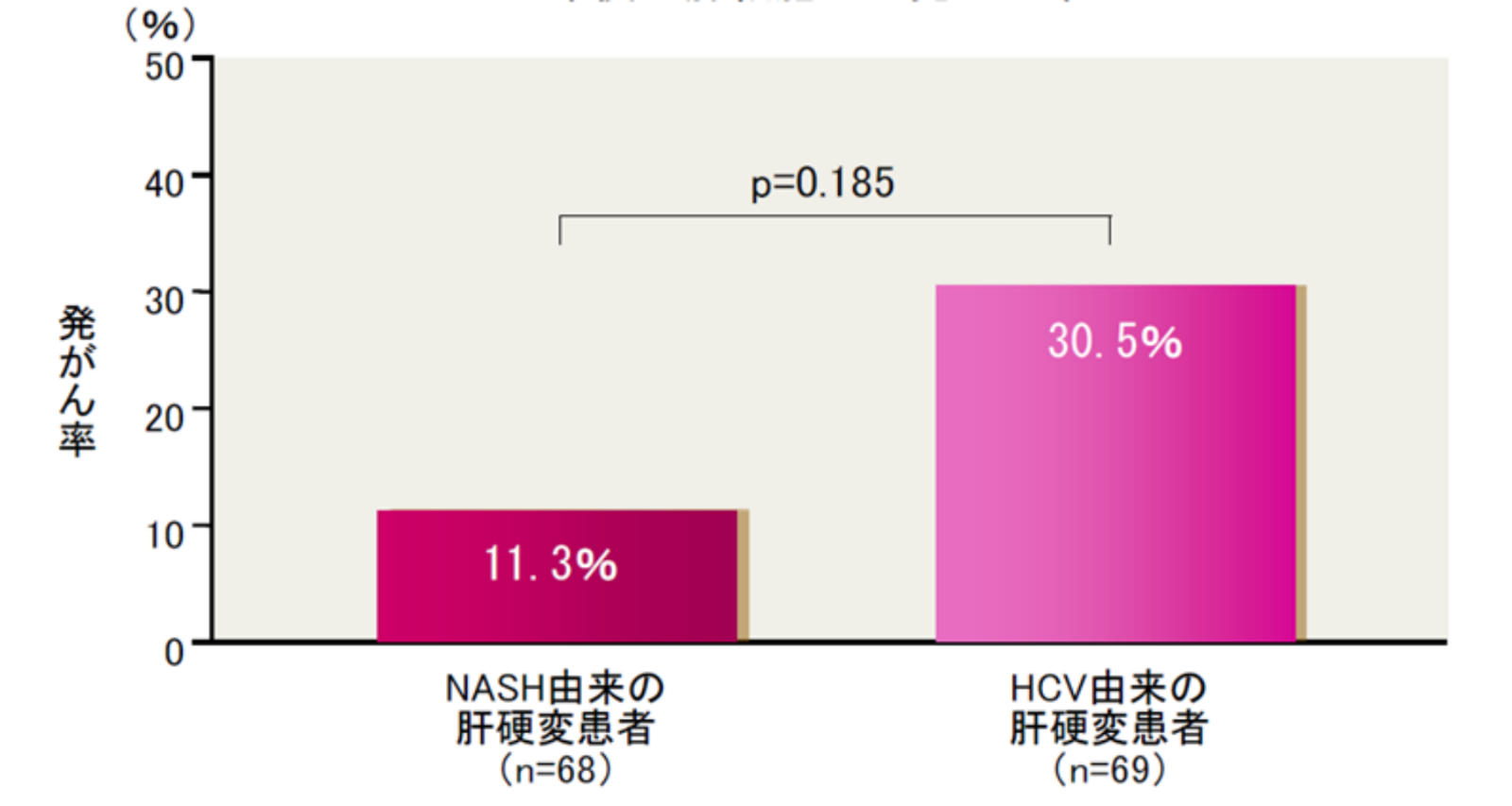
なお、NAFLDの中でも繊維化ステージが3もしくは4に該当する高度繊維化を有するハイリスクのNAFLDは、①心血管イベント発症率が高い、②非代償性肝硬変へと移行しやすい、③肝細胞癌の発症率が高い、などといった特徴を有します。NASHから発癌した肝臓癌における腫瘍マーカー検査では、ウィルス肝炎と比較して、αフェトプロテインの陽性率が低く、PIVKA-IIの陽性率が高い特徴があります。
NAFLDの頻度について検討した研究は様々なものがあり、例えば、約4万人の健康診断受診者を対象とした検討では、超音波で診断したNAFLDの頻度は男性で20.8%、女性で12.8%、日本人間ドック学会の検討では成人男性の約30%、成人女性の約20%、8,000人以上を対象とした大規模研究では、男女合わせて約30%と報告されており、この結果はアジアの有病率とほぼ同等です。
NAFLDの頻度の国際比較
(Younossi Z, et al. Hepatology 2016より引用)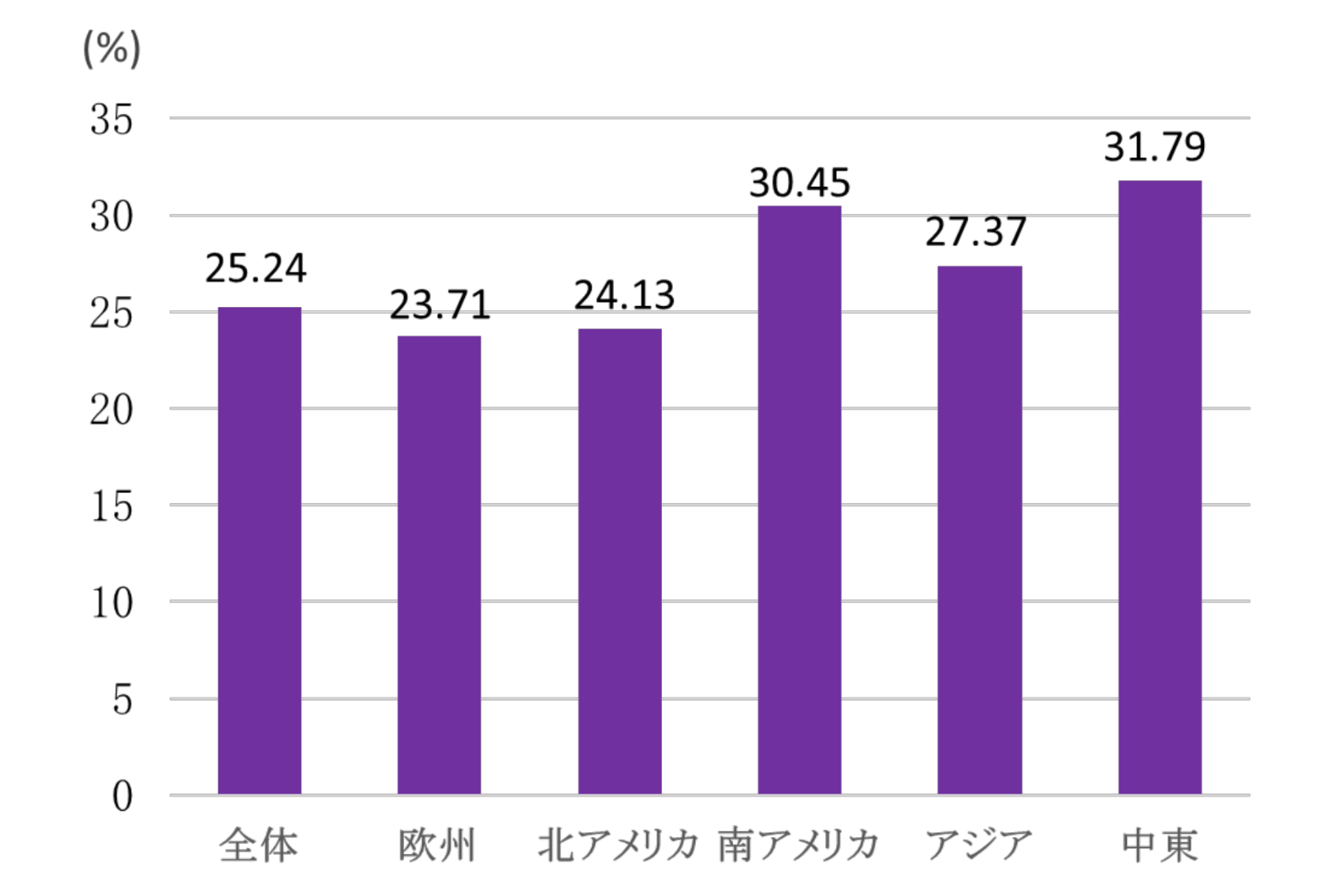
NAFLD/NASHにおけるメタボリックシンドロームの合併率はNAFLDで40%、NASHで50%であり、メタボリックシンドロームの構成要因となる生活習慣病の合併も30%~70%に見られており、複数の大規模コホート研究からもNAFLD患者数の増加とメタボリックシンドローム患者数の増加との深い関連が示されています。また肥満そのものとNAFLD/NASHについても深い関連があり、BMIが23kg/m2未満の非肥満者におけるNAFLD/NASHの合併率が10%以下であるのに対し、BMIが30kg/m2以上の高度肥満においては、その合併率は約80%であることが報告されています。
2型糖尿病におけるNASH/NAFLDの罹患率
(Younossi Z, et al. J Hepatol 2019より引用)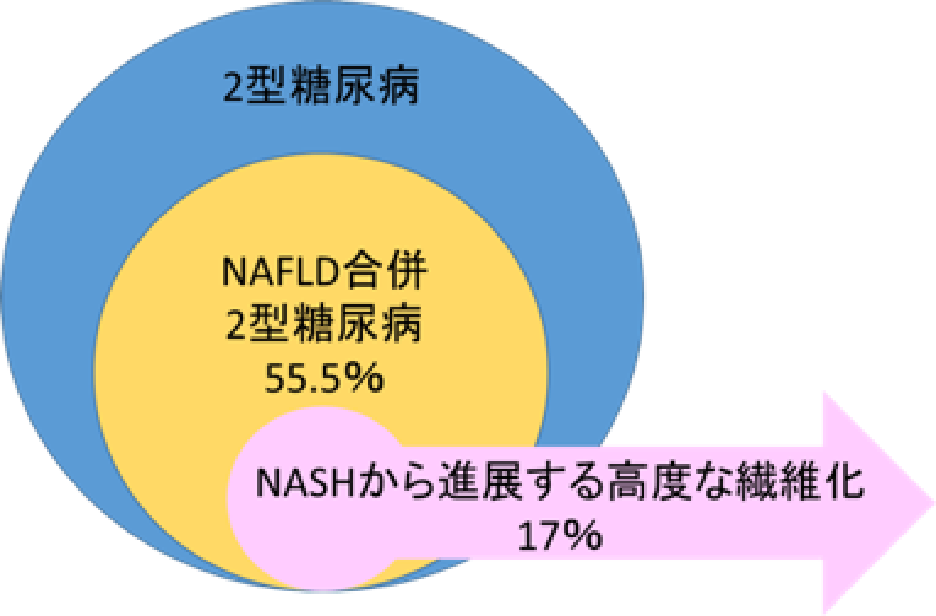
しかしながら、NAFLDは生活習慣病など後天的な環境要因の影響が強いものの、家族内に集積することや、一卵性双生児の研究などから、病態形成には先天的な遺伝的要因の関与も大きいことも知られており、近年、非肥満者のNAFLD/NASH合併も肥満者のNAFLD/NASH合併と同様に注目されています。特に肥満の程度に比べて臓器障害が強く発症する傾向があるアジア人においては、NAFLD患者の30%~70%程度が非肥満者との報告があります。これまで、NAFLDの発症に関連する遺伝子多型として、PNPLA3やTM6SF2をはじめとするいくつかの多型が国内外の研究で報告されており、これらのリスクアリル保有率の高い地域では、非肥満NAFLDの頻度が高いことが知られています。本邦における非肥満者でのNAFLD合併率は15.2%と報告されており、非肥満者におけるNAFLD合併の独立危険因子としては、①20歳時より10kg以上の体重増加、②週3回以上の就寝前2時間以内の食事摂取、③純エタノール換算20g/日未満のアルコール摂取の3項目があげられています。
繊維化のステージごとの肝関連死亡のリスク比
(Dulai PS, et al. Hepatology 2017より引用)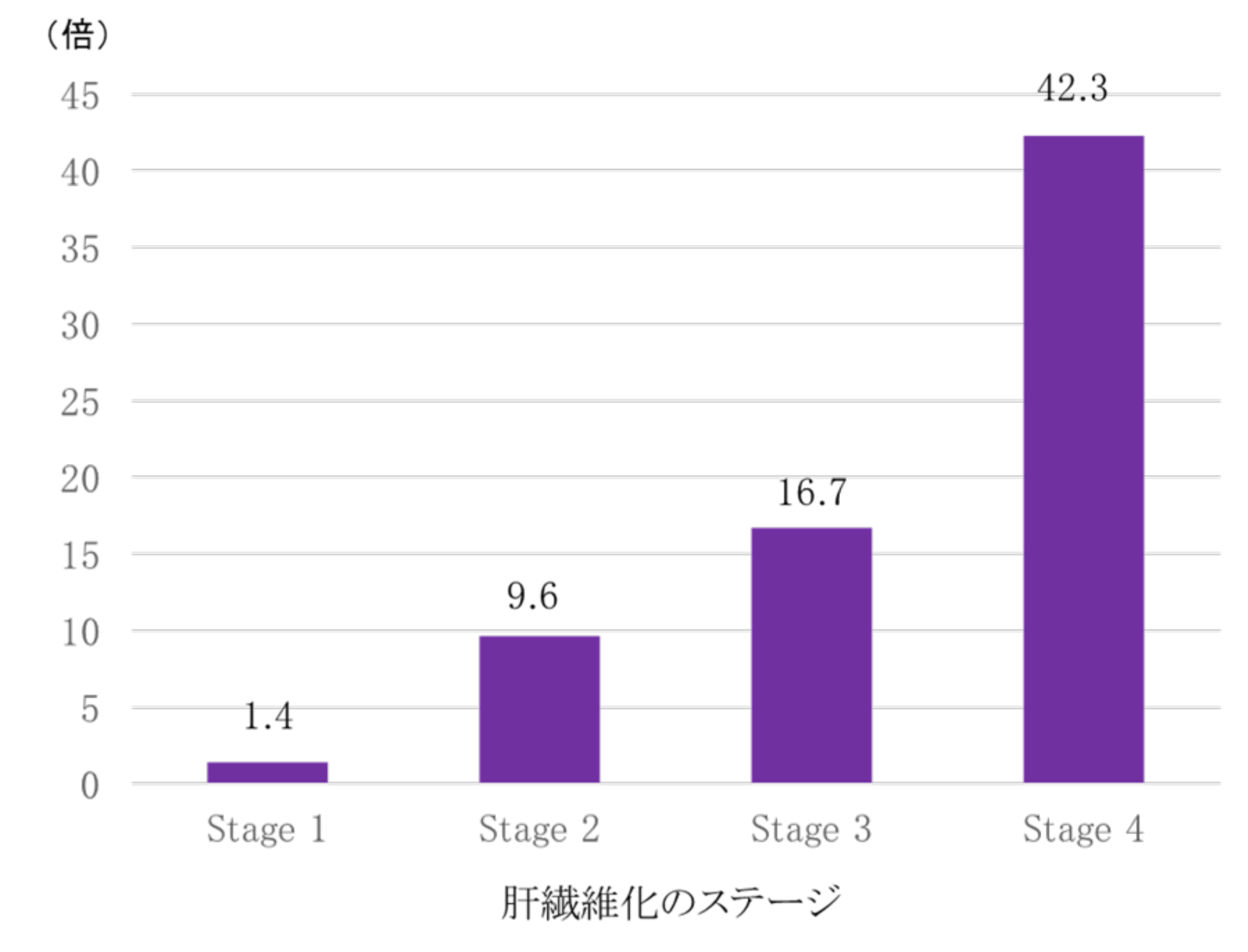
NAFLD/NASHは毎年患者数が増加しており、肝関連死や心血管イベントによる死亡リスクが高いため、その死亡率は一般住民と比較して1.3倍~1.8倍に上昇します。そのため、予後改善を目指して世界中で肝繊維化治療や発癌予防の研究と開発が行われていますが、現在NASHの保険適応を認められた治療薬は国内外でまだありません。そのため実臨床においては、NASHの背景にあるメタボリックシンドロームの基礎疾患である糖尿病、脂質異常症、高血圧などに対する薬物療法が考慮されています。
SGLT-2阻害薬のNAFLDに対する効果
(Sumida Y, et al. Hepatol Res 2019より引用)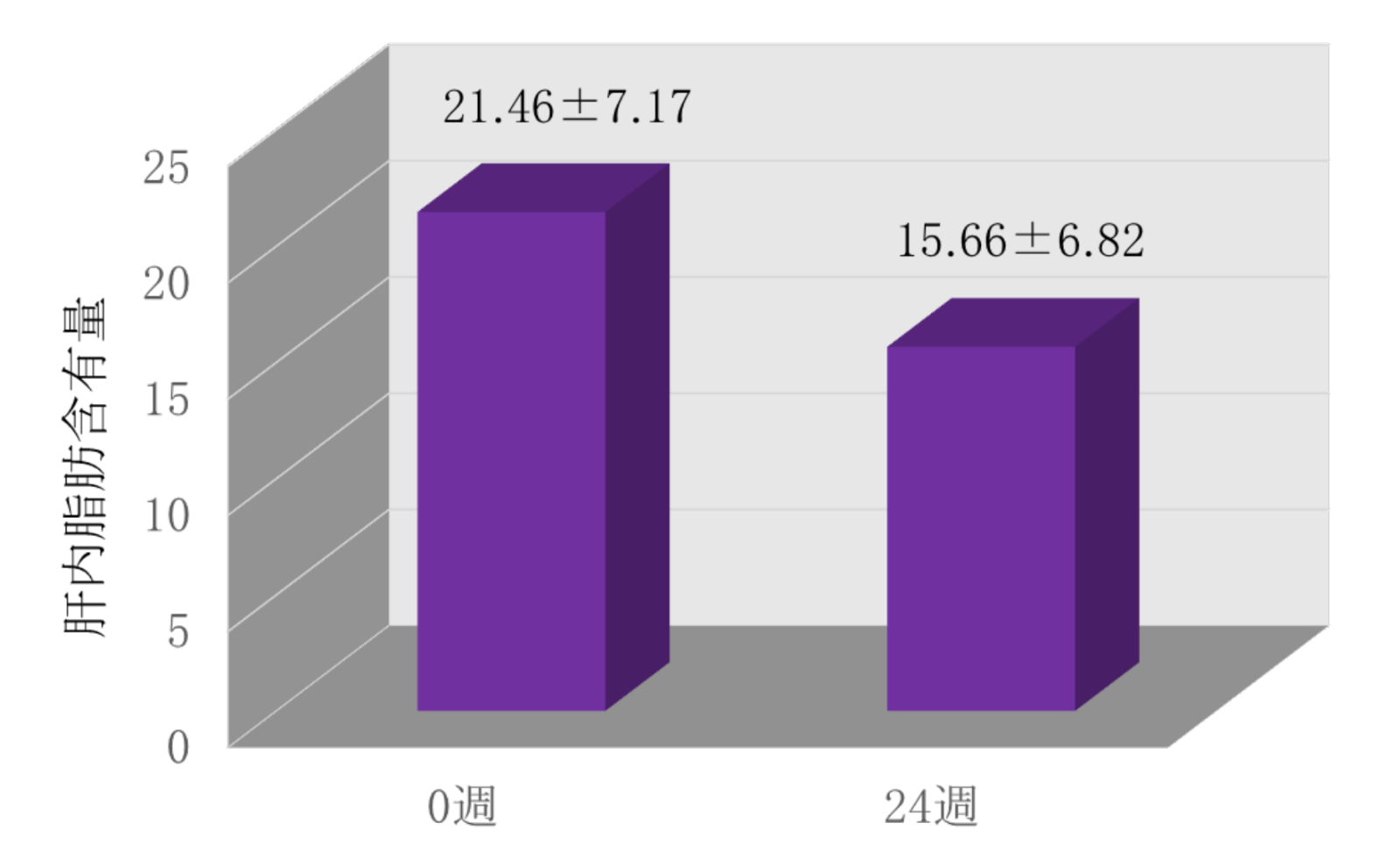
『非アルコール性脂肪性肝疾患の治療』
NAFLDは肥満との関連が極めて強い病態であるため、食事療法や運動療法による減量で内臓脂肪を是正することが治療においては一番大事で、栄養指導による減量可能例では、ほぼ全例で肝機能障害が改善し、約60%の症例で脂肪肝が改善したとの報告もあります。なお、BMIが正常域の非肥満の患者においても、内臓肥満例は少なくないため減量が必要です。減量の効果については、体重の3%の減量で脂肪変性が消失、5%では炎症と肝細胞の風船様変性が改善、そして7%ではNASHが改善すると報告されています。また、睡眠時無呼吸症候群の合併例においては、無呼吸時の低酸素がNASHを増悪させるとの報告もあるため、睡眠時無呼吸症候群の治療も必要になります。
BMI別のNAFLD有病率
(Eguchi Y, et al. J Gastroenterol 2012より引用)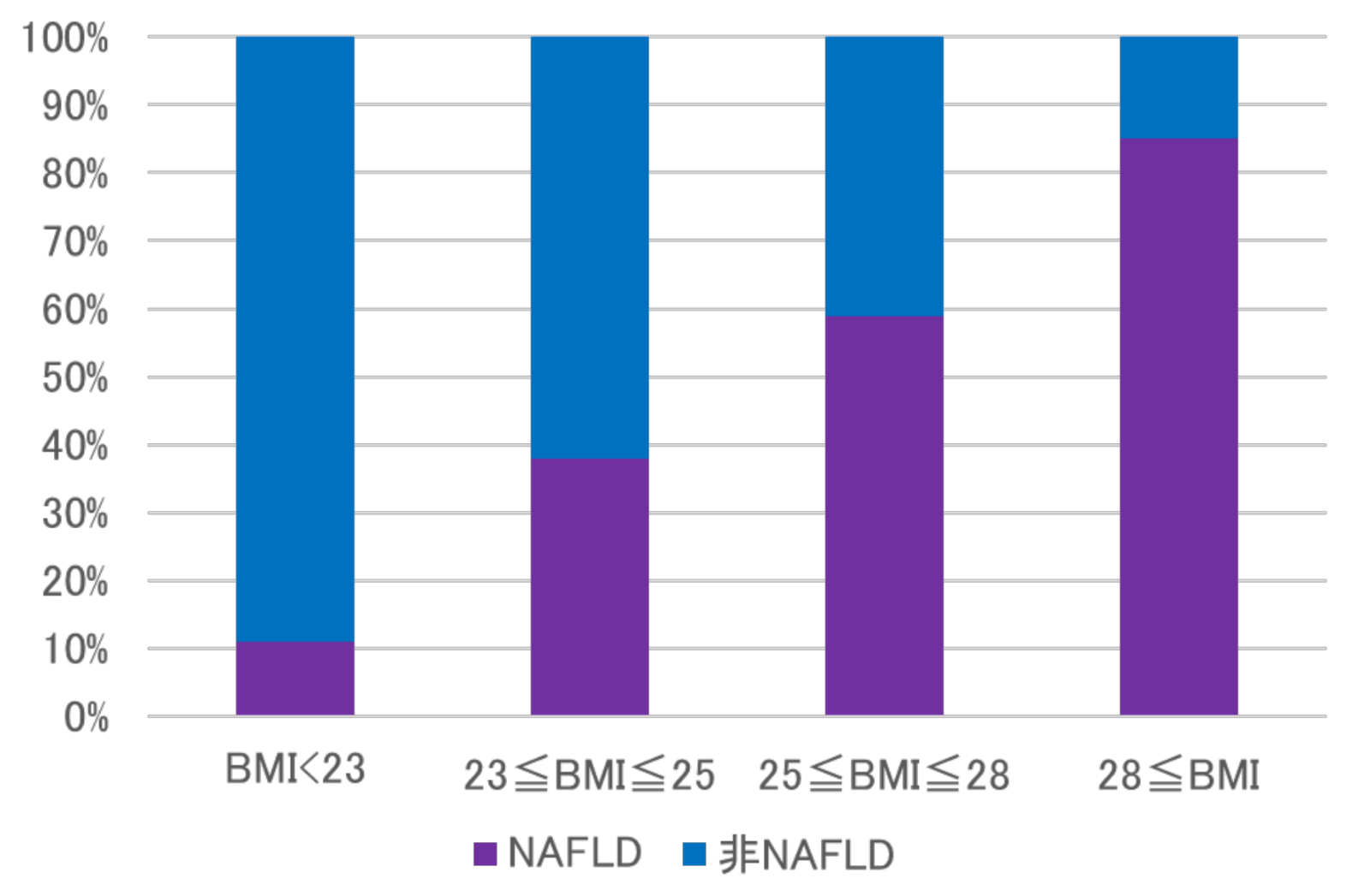
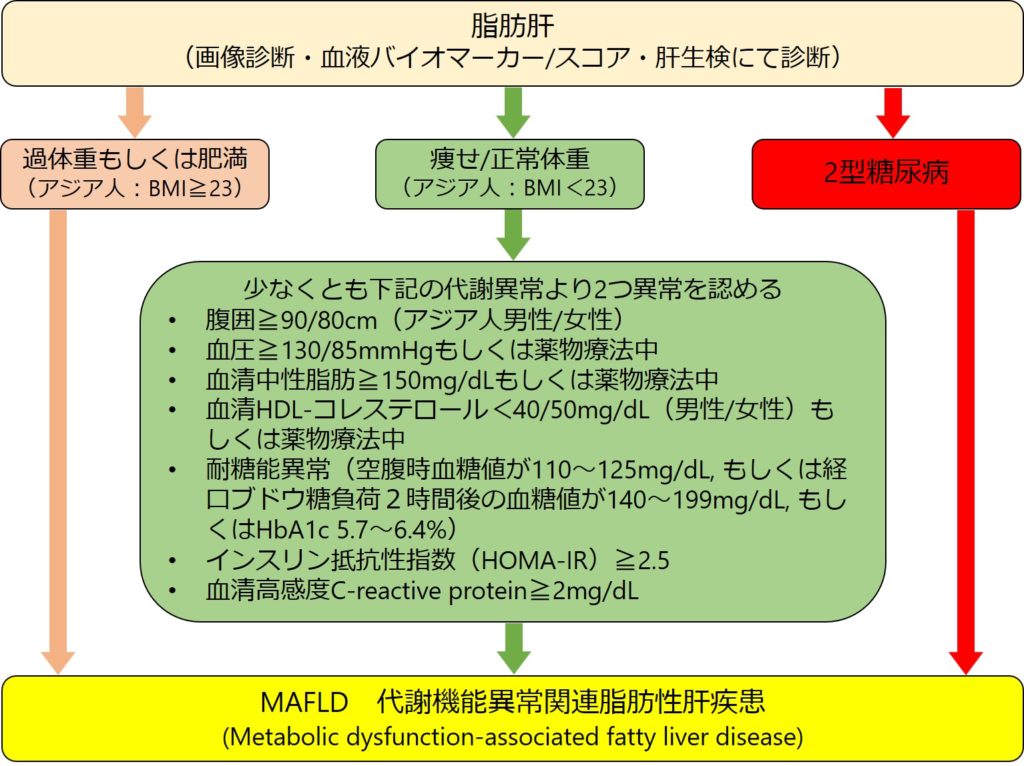
『代謝機能障害関連脂肪性肝疾患』
脂肪肝の患者の多くは肥満や耐糖能異常、高血圧などの代謝異常を合併しており、これらの代謝異常は肝線維化の進展、動脈硬化性心血管疾患や患者予後に深く関わることが明らかになってきています。そのため、代謝異常を合併する脂肪肝のことを代謝機能障害関連脂肪性肝疾患 (metabolic dysfunction-associated fatty liver disease : MAFLD) と命名し、その診断基準が提唱されています。代謝異常の合併とは、過体重や肥満、2型糖尿病のほかに、腹部肥満、中性脂肪高値、善玉コレステロール(HDL-C)低値、血圧高値、インスリン抵抗性、全身性炎症などが複数あてはまる場合を指します。
このMASLDに該当して、かつ肝炎が生じている場合には、代謝異常関連脂肪肝炎( Metabolic Dysfunction Associated Steatohepatitis: MASH )と診断されます。
MASLD 代謝機能障害関連脂肪性肝疾患